-
 Registracija
Registracija
-
 Nacionalinis vėžio centras
Nacionalinis vėžio centras
-
 Nacionalinis vėžio institutas
Nacionalinis vėžio institutas
- Titulinis
- Nacionalinis vėžio centras
- Klinikiniai tyrimai
Klinikiniai tyrimai
• Visuose klinikiniuose tyrimuose nurodoma, kas gali būti tiriamuoju. Kiekvienu atveju yra labai griežti reikalavimai, vadinami “įtraukimo kriterijai”, kuriuos pacientas turi atitikti, norėdamas dalyvauti tyrime. Pavyzdžiui, būna nurodoma, kad tyrime gali dalyvauti tik tam tikros stadijos vėžiu sergantys pacientai, gavę tam tikrą gydymą, ir panašiai. Taip pat kiekviename tyrime nurodomi “neįtraukimo kriterijai”, kuriems esant pacientas dalyvauti tyrime negali. Tai gali būti, pavyzdžiui, netinkamas amžius, gretutinės ligos, blogi kraujo tyrimų rodikliai ar kita.
• Jei klinikiniame tyrime tiriamas vaistas (ar diagnostikos metodas) pasirodo veiksmingas ir saugus, jis patenka į rinką, juo pradedama gydyti daugiau pacientų (arba tyrimas pradedamas plačiai naudoti praktikoje). Tokiu būdu vyksta medicinos mokslo pažanga. Klinikiniame tyrime dalyvauja iki kelių tūkstančių tiriamųjų skirtingose valstybėse. Tokie daugiacentriai tyrimai atliekami dėl to, kad per trumpesnį laikotarpį į tyrimą būtų įtrauktas reikiamas pacientų skaičius ir rezultatai būtų patikimesni.
• Galite klausti gydytojo įvairiausių jums rūpimų klausimų. Svarbiausius ir dažniausiai pateikiamus nurodome žemiau:
• Kiek laiko truks tyrimas?
• Kaip vyks tyrimas? Kiek kartų turėsiu lankytis pas gydytoją, kokius tyrimus turėsiu atlikti? Ar galėsiu įprastai gyventi, dirbti?
• Kur tyrimas pradėtas? Kokios šalys jame dalyvauja? Kiek pacientų dalyvauja ar planuoja dalyvauti?
• Koks gydymas (ar tyrimas) bus naudojamas?
• Koks pagrindinis tyrimo tikslas?
• Kaip bus užtikrinamas tyrimo saugumas?
• Ar yra kokia nors rizika dalyvauti tyrime?
• Kokia nauda dalyvauti tyrime?
• Kokie yra kiti galimi gydymo ar tyrimo metodai?
• Ar reikės mokėti už dalyvavimą tyrime? Už tyrimus?
• Kaip man bus atlyginama žala, jei ji bus padaryta? Ar yra draudimas, ištikus komplikacijoms?
• Ar bus galima tęsti gydymą pasibaigus klinikiniam tyrimui?
• Ar galima nutraukti dalyvavimą tyrime bet kuriuo metu?
• Klinikiniai tyrimai leidžiami tik tuomet, kai neabejojama jų moksline ir praktine verte, kai garantuojama tiriamojo interesų apsauga bei informacijos apie tiriamąjį konfidencialumas. Būtinas savanoriškas tiriamojo asmens sutikimas dalvauti tyrime.
• Asmuo, kuriam pasiūloma dalyvauti tyrime, turi žinoti, kad tik jis pats nusprendžia dalyvauti tyrime, ar ne. Prieš įtraukiant į tyrimą, asmeniui turi būti pateikiamas dokumentas su visa svarbiausia informacija. Dokumentas vadinamas Asmens informavimo ir informuoto asmens sutikimo forma. Šioje formoje išdėstoma informacija apie tyrimo tikslą, planą, taikomus metodus, naudą, galimą riziką, žalos atlyginimą.
• Tyrimo metu garantuojamas informacijos apie tiriamojo sveikatą konfidencialumas. Priimant sprendimą dėl dalyvavimo tyrime, nereikia skubėti, būtina perskaityti informaciją bei pasitarti su gydytoju ir išsiaiškinti visus rūpimus klausimus. Esant reikalui, galima pasitarti su giminėmis ar kitais asmenimis.
Galima nauda dalyvauti tyrime:
• Aktyviai dalyvausite sveikatos apsaugos veikloje, kuri vyksta visame pasaulyje.
• Turėsite galimybę gauti naujausią gydymą, taikomą pasaulyje.
• Turėsite galimybę gauti pačią geriausią medicininę priežiūrą, jums bus atliekama daugiau tyrimų ir jūs būsite atidžiau stebimas, nei įprastai gydant ligą.
• Padėsite kitiems, sergantiems ar susirgsiantiems ta pačia liga.
Galima rizika:
• Gali pasireikšti netikėtas nepageidaujanmas tiriamojo gydymo (vaisto) poveikis.
• Tiriamasis gydymas gali nebūti geresnis už jau žinomą ar jums jau taikytą gydymą.
• Dalyvavimas tyrime gali pareikalauti daugiau laiko vizitams pas gydytoją, ilgesnės hospitalizacijos ar papildomų tyrimų, numatytų tyrimo protokole.
• Informaciją apie tyrime dalyvaujantį asmenį turi tik pagrindinis tyrėjas. Visa informacija, siunčiama tyrimo užsakovui, yra koduota. Tyrimo eigoje ir pabaigoje mokslo žurnaluose viešinama mokslinė informacija apie tyrimą, nurodomi rezultatai, nenurodant jokios informacijos apie konkrečius tyrime dalyvaujančius asmenis.
• Po tyrimo vertinami rezultatai ir sprendžiama, ar tyrimą tęsti ar pabaigti. Jei vaistas patvirtinamas naudoti nuolat, gali būti toliau tęsiami klinikiniai tyrimai lyginant tiriamojo vaisto veikimą su kitų, jau esamų vaistų.
| Grupė | Melanoma |
| Tyrimo pavadinimas, protokolo nr. | Atsitiktinių imčių, lygiagrečių grupių tyrimas, skirtas palyginti GME75. Protokolo Nr. CGME751A12101 |
| Fazė | I |
| Indikacija | IIB, IIC, III st. melanoma, 2-13 sav. po rezekcijos |
| Intervencija | GME751/Pembrolizumab |
| Komanda | PI-V. Urbonas. Koordinatoriai- A. Šukštienė, I.R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 8 |
| Tyrimo pabaiga | 2025-06 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Melanoma |
| Tyrimo pavadinimas, protokolo nr. | Atsitiktinių imčių dvigubai aklas tyrimas, kuriame vertinamas ABP 206 farmakokinetinis panašumas, palyginti su OPDIVO® (nivolumabu), gydant III ar IV stadijos melanomos pacientus, kuriems taikoma adjuvantinė terapija. Protokolo Nr. 20220083 |
| Fazė | III |
| Indikacija | Adjuvantas, kai radikaliai rezekuota III arba IV stadija |
| Intervencija | Nivolumabas vs biosimiliarus Nivolumabas |
| Komanda | PI-V. Urbonas, Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | Gydymas |
| Tyrimo pabaiga | 2024-10-11 |
| Įtraukimą Vykdantis | Ne |
| Grupė | Melanoma |
| Tyrimo pavadinimas, protokolo nr. | Atviras I fazės daugiacentris, randomizuotas, dvigubai aklas tyrimas, kuriame vertinamas ABP 206 farmakokinetinis panašumas, palyginti su OPDIVO® (Nivolumabu), skirto III ar IV stadijos melanomai, sergantiems rezekuotomis melanomomis adjuvantinėje aplinkoje. Protokolo Nr. NECVAX-NEO1-LT |
| Fazė | I |
| Indikacija | Bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST |
| Intervencija | Papildoma geriamoji vakcina |
| Komanda | PI-V. Urbonas. Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 6 |
| Tyrimo pabaiga | 2026-11 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Melanoma |
| Tyrimo pavadinimas, protokolo nr. | Epigenetiniai kraujyje laisvai cirkuliuojančios DNR žymenys ankstyvajai vėžio atkryčio diagnostikai. Protokolo Nr. EpiCancer2023 |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Planuojama perioperacinė chemoterapija |
| Intervencija | Kraujo ėminiai cfDNR nustatyti |
| Komanda | PI - A. Dulskas, Koordinatorius - N. Kravčenko |
| Tyrimo būsena / Liko vietų | 20 |
| Tyrimo pabaiga | 2028 m. |
| Įtraukimą Vykdantis | Taip |
| Grupė | Kiaušidžių vėžys |
| Tyrimo pavadinimas, protokolo nr. | Atsitiktinių imčių klinikinis tyrimas palaikomajai terapijai olaparibu, durvalumabu, NSGO-CTU-DOVACC. Protokolo Nr. NSGO-CTU-DOVACC |
| Fazė | III |
| Indikacija | Platinai jautrus, I arba II atkrytis, BRCA (-) |
| Intervencija | Palaikomasis gydymas olaparibu+/-durvaliumabu+/-UV1 |
| Komanda | PI- B. Brasiūnienė; Koordinatorius A. Šukštienė |
| Tyrimo būsena / Liko vietų | 3 |
| Tyrimo pabaiga | 2026-12 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Melanoma |
| Tyrimo pavadinimas, protokolo nr. | Atsitiktinių imčių dvigubai aklas tyrimas, kuriame vertinamas ABP 206 veiksmingumas, saugumas ir imunogeniškumas, palyginti su OPDIVO® (nivolumabu) gydymui nepasirengusiems asmenims, sergantiems neišplitusia ar metastazavusia melanoma. Protokolo Nr. 20210031 |
| Fazė | III |
| Indikacija | I eilė, kai nerezektabili III / IV st |
| Intervencija | Nivolumabas vs biosimiliarus Nivolumabas |
| Komanda | PI-V. Urbonas. Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 6 |
| Tyrimo pabaiga | 2025-01 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Krūties vėžys |
| Tyrimo pavadinimas, protokolo nr. | CHAIMELEON dirbtinio intelekto įrankių perkėlimo iš laboratorijos į rinką spartinimas vėžio valdymui. Protokolo Nr. CHAIMELEON |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Krūties Ca |
| Intervencija | Radiologinių vaizdų ir klinik. duomenų surinkimas |
| Komanda | PI-J. Ušinskienė; Koordinatorius - I.R.Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 995 |
| Tyrimo pabaiga | 2025 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Krūties vėžys |
| Tyrimo pavadinimas, protokolo nr. | Atsitiktinių imčių III fazės tyrimas, pažasties operacija su pažasties limfmazgių, TAXIS |
| Fazė | III |
| Indikacija | Krūties Ca su kliniškai pakenktais lm |
| Intervencija | Operacija su pažasties lm disekcija arba be jos, po kurios taikoma spindulinė terapija |
| Komanda | PI- V. Ostapenko; Koordinatorius A. Šukštienė |
| Tyrimo būsena / Liko vietų | 44 |
| Tyrimo pabaiga | 2024-12 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Krūties vėžys |
| Tyrimo pavadinimas, protokolo nr. | Pažasties limfmazgių disekcijos sąsaja su onkologiniu saugumu pacientams. Protokolo Nr. OPBC-07/microNAC |
| Fazė | III |
| Indikacija | Krūties Ca, kai nustatoma likusių mikrometastazių po neoadjuvantinės chemoterapijos, kai taikyta pažasties disekacija arba be jos. |
| Intervencija | Duomenų rinkimas |
| Komanda | PI- V. Ostapenko; Koordinatorius I. R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 24 |
| Tyrimo pabaiga | 2024-12 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Skrandžio vėžys |
| Tyrimo pavadinimas, protokolo nr. | PIPAC |
| Fazė | Pilotinis |
| Indikacija | I eilė, HER2(-), metastazes tik pilvaplėvėje |
| Intervencija | PIPAC + FOLFOX |
| Komanda | PI – A. Baušys, Koordinatorius A. Šukštienė |
| Tyrimo būsena / Liko vietų | 15 |
| Tyrimo pabaiga | 2024 m. |
| Įtraukimą Vykdantis | Taip |
| Grupė | Skrandžio vėžys |
| Tyrimo pavadinimas, protokolo nr. | Epigenetiniai kraujyje laisvai cirkuliuojančios DNR žymenys ankstyvajai vėžio atkryčio diagnostikai. Protokolo Nr. EpiCancer2023 |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Planuojama perioperacinė chemoterapija |
| Intervencija | Kraujo ėminiai cfDNR nustatyti |
| Komanda | PI- A. Dulskas. Koordinatorius N. Kravčenko |
| Tyrimo būsena / Liko vietų | 20 |
| Tyrimo pabaiga | 2028 m. |
| Įtraukimą Vykdantis | Taip |
| Grupė | Storosios žarnos ir plonosios žarnos vėžys |
| Tyrimo pavadinimas, protokolo nr. | Epigenetiniai kraujyje laisvai cirkuliuojančios DNR žymenys ankstyvajai vėžio atkryčio diagnostikai. Protokolo Nr. EpiCancer2023. |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Planuojama neoadjuvantinė chemoterapija |
| Intervencija | Kraujo ėminiai cfDNR nustatyti |
| Komanda | PI - A. Dulskas. Koordinatorius N. Kravčenko |
| Tyrimo būsena / Liko vietų | 20 |
| Tyrimo pabaiga | 2028 m. |
| Įtraukimą Vykdantis | Taip |
| Grupė | Storosios žarnos ir plonosios žarnos vėžys |
| Tyrimo pavadinimas, protokolo nr. | CHAIMELEON dirbtinio intelekto įrankių perkėlimo iš laboratorijos į rinką spartinimas vėžio valdymui. Protokolo Nr. CHAIMELEON |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Storosios žarnos ir plonosios žarnos vėžio Ca |
| Intervencija | Radiologinių vaizdų ir klinik. duomenų surinkimas |
| Komanda | PI-J. Ušinskienė. Koordinatorius - I.R.Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 995 |
| Tyrimo pabaiga | 2025 m. |
| Įtraukimą Vykdantis | Taip |
| Grupė | Galvos kaklo vėžys |
| Tyrimo pavadinimas, protokolo nr. | Atviras I fazės daugiacentris, randomizuotas, dvigubai aklas tyrimas, kuriame vertinamas ABP 206 farmakokinetinis panašumas, palyginti su OPDIVO® (Nivolumabu), skirto III ar IV stadijos melanomai, sergantiems rezekuotomis melanomomis adjuvantinėje aplinkoje. Protokolo Nr. NECVAX-NEO1-LT |
| Fazė | I |
| Indikacija | Bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST |
| Intervencija | Papildoma geriamoji vakcina |
| Komanda | PI-V. Urbonas; Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 6 |
| Tyrimo pabaiga | 2026-11 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Prostatos vėžys |
| Tyrimo pavadinimas, protokolo nr. | CHAIMELEON dirbtinio intelekto įrankių perkėlimo iš laboratorijos į rinką spartinimas vėžio valdymui. Protokolo Nr. CHAIMELEON |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Prostatos Ca |
| Intervencija | Radiologinių vaizdų ir klinik. duomenų surinkimas |
| Komanda | PI-J. Ušinskienė. Koordinatorius - I.R.Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 995 |
| Tyrimo pabaiga | 2025 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Prostatos vėžys |
| Tyrimo pavadinimas, protokolo nr. | 3 fazės, atsitiktinių imčių, atviras MK-5684 ir alternatyvaus preparato abiraterono acetato arba enzalutamido tyrimas, skirtas tiriamiesiems, sergantiems metastazavusiu, kastracijai atspariu prostatos vėžiu (mKAPV), progresavusiu po ankstesnio gydymo vienu naujos kartos hormoniniu preparatu (NKHP) Protokolo Nr. MK5684-004 |
| Fazė | III |
| Indikacija | Kastracijai atsparus prostatos vėžys (mKAPV), progresavęs po ankstesnio gydymo vienu naujos kartos hormoniniu preparatu (NKHP) |
| Intervencija | MK-5684, abiraterono acetatas arba enzalutamidas |
| Komanda | PI - A. Ulys. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | 9 |
| Tyrimo pabaiga | 2026 m. |
| Įtraukimą Vykdantis | Taip |
| Grupė | Inkstų vėžys |
| Tyrimo pavadinimas, protokolo nr. | Atviras I fazės daugiacentris, randomizuotas, dvigubai aklas tyrimas, kuriame vertinamas ABP 206 farmakokinetinis panašumas, palyginti su OPDIVO® (Nivolumabu), skirto III ar IV stadijos melanomai, sergantiems rezekuotomis melanomomis adjuvantinėje aplinkoje. Protokolo Nr. NECVAX-NEO1-LT |
| Fazė | I |
| Indikacija | Bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST |
| Intervencija | Papildoma geriamoji vakcina |
| Komanda | PI-V. Urbonas; Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 6 |
| Tyrimo pabaiga | 2026-11 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Plaučių vėžys |
| Tyrimo pavadinimas, protokolo nr. | 3 fazės, atsitiktinių imčių, dvigubai koduotas, placebu ir aktyviuoju palyginamuoju preparatu kontroliuojamas klinikinis tyrimas, skirtas palyginti adjuvanto V940 (mRNR-4157) skyrimą kartu su pembrolizumabu ir adjuvanto placebo skyrimą kartu su pembrolizumabu dalyviams, sergantiems rezekuotu II, IIIA, IIIB (N2) stadijos nesmulkiųjų ląstelių plaučių vėžiu. Protokolo Nr. V940-002 |
| Fazė | III |
| Indikacija | NSLPV, išoperuotas (R0) II, IIIA, IIIB st, N2, I eilė |
| Intervencija | V940 + Pembro |
| Komanda | PI- V. Gedvilaitė. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | 4 |
| Tyrimo pabaiga | 2025 m. |
| Įtraukimą Vykdantis | Taip |
| Grupė | Plaučių vėžys |
| Tyrimo pavadinimas, protokolo nr. | Atviras I fazės daugiacentris, randomizuotas, dvigubai aklas tyrimas, kuriame vertinamas ABP 206 farmakokinetinis panašumas, palyginti su OPDIVO® (Nivolumabu), skirto III ar IV stadijos melanomai, sergantiems rezekuotomis melanomomis adjuvantinėje aplinkoje. Protokolo Nr. NECVAX-NEO1-LT Protokolo Nr. NECVAX-NEO1-LT |
| Fazė | I |
| Indikacija | NSCLC bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST |
| Intervencija | Papildoma geriamoji vakcina |
| Komanda | PI-V. Urbonas; Sub-I - E. Baltruškevičienė, L. Gatijatullin; Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 6 |
| Tyrimo pabaiga | 2026-11 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Plaučių vėžys |
| Tyrimo pavadinimas, protokolo nr. | CHAIMELEON dirbtinio intelekto įrankių perkėlimo iš laboratorijos į rinką spartinimas vėžio valdymui. Protokolo Nr. CHAIMELEON |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Plaučių Ca |
| Intervencija | Radiologinių vaizdų ir klinik. duomenų surinkimas |
| Komanda | PI-J. Ušinskienė. Koordinatorius - I. R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 995 |
| Tyrimo pabaiga | 2025 m. |
| Įtraukimą Vykdantis | Taip |
| Grupė | Plaučių vėžys |
| Tyrimo pavadinimas, protokolo nr. | Atviras, daugiacentris, 3 fazės atsitiktinių imčių, aktyviais lyginamaisiais metodais kontroliuojamas klinikinis tyrimas Pembrolizumabo (MK-3475) derinyje su Sacituzumab Govitecan, palyginti su MK-3475 monoterapija, kaip pirmos eilės gydymu sergant PD L1 TPS didesnis arba lygus 50 % metastazavusiu nesmulkialąsteliniu plaučių vėžiu (KEYNOTE D46/EVOKE-03). Protokolo Nr. MK-3475-D46 |
| Fazė | III |
| Indikacija | NSLPV, IV st, PD-L1>50%, I eilė |
| Intervencija | Pembro+sacituzumab govitekan |
| Komanda | PI – S. Cicėnas. Koordinatoriai - A. Šukštienė, I. R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 5 |
| Tyrimo pabaiga | 2025-03 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Kiti solidiniai navikai |
| Tyrimo pavadinimas, protokolo nr. | Atvirasis, I fazės daugiacentris, klinikinis tyrimas siekiant įvertinti NECVAX-NEO1, Protokolo Nr. NECVAX-NEO1-LT |
| Fazė | I |
| Indikacija | Bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST |
| Intervencija | Papildoma geriamoji vakcina |
| Komanda | PI-V. Urbonas; Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 6 |
| Tyrimo pabaiga | 2026-11 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Kiti solidiniai navikai |
| Tyrimo pavadinimas, protokolo nr. | Europos onkologinio gyvenimo kokybės priemonių rinkinio patvirtinimas. Europos pilotinė apklausa. Protokolo Nr. EUonQoL |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Kiti solidiniai navikai - aktyvus gydymas, stebėsena arba paliatyvus gydymas |
| Intervencija | Neintervencinis, stebimasis |
| Komanda | PI- A. Dulskas; Koordinatoriai N. Kravčenko, I. R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 79 |
| Tyrimo pabaiga | 2024-11 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Gimdos kūno vėžys |
| Tyrimo pavadinimas, protokolo nr. | II/III fazės navtemadlino kaip palaikomojo gydymo tyrimas pacientėms, sergančioms laukinio tipo TP53 (TP53WT) pažengusiu ar atsinaujinusiu endometriumo vėžiu, kurios reagavo į chemoterapiją. Protokolo Nr. KRT-232-118 |
| Fazė | II/III |
| Indikacija | TP53WT, pirminė išplitusi liga arba atkrytis, Pravesti iki 6 ciklų TP chemoterapijos ir pasiektas CR arba PR pagal RECIST |
| Intervencija | Palaikomasis gydymas navtemadlinu |
| Komanda | PI- B. Brasiūnienė. Koordinatoriai N. Kravčenko, A. Šukštienė |
| Tyrimo būsena / Liko vietų | Vyksta duomenų apdorojimas |
| Tyrimo pabaiga | Sustabdytas tyrimas 2024-07-29 |
| Įtraukimą Vykdantis | Ne |
| Grupė | Gimdos gleivinės vėžys |
| Tyrimo pavadinimas, protokolo nr. | Gimdos gleivinės (endometriumo) vėžio nustatymas taikant gimdos kaklelio DNR metilinimo tyrimus. Protokolo Nr. Endo-cancer-2022 |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Biožymenų |
| Intervencija | Gimdos gleivinės vėžio pacientų mėginių rinkimas. Suplanuota, bet dar neįvykusi visiška histerektomija |
| Komanda | PI- R. Čiurlienė. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Vyksta duomenų apdorojimas |
| Tyrimo pabaiga | 2025 m. |
| Įtraukimą Vykdantis | Ne |
| Grupė | Kiaušidžių vėžys |
| Tyrimo pavadinimas, protokolo nr. | Chemoimunoterapijos, taikant autologinius dendritinių ląstelių preparatus, saugumo tyrimas, gydant pacientes, sergančias 3 stadijos kiaušidžių vėžiu. Protokolo Nr. ChImDLP-2 |
| Fazė | I/II |
| Indikacija | Atlikta optimali citoredukcija (R0). Indikuotina pooperacinė chemoterapija karboplatinos ir paklitakselio deriniu. |
| Intervencija | Dendritinių ląstelių preparatas (DLP) |
| Komanda | PI-B. Intaitė. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Tyrimas sustabdytas. Vyksta duomenų apdorojimas |
| Tyrimo pabaiga | 2026 m. |
| Įtraukimą Vykdantis | Ne |
| Grupė | Kiaušidžių vėžys |
| Tyrimo pavadinimas, protokolo nr. | Atezolizumabo derinys su bevacizumabu ir chemoterapija, lyginant su bevacizumabu ir chemoterapija, atsinaujinus kiaušidžių vėžiui – atsitiktinių imčių, III fazės tyrimas. Protokolo Nr. AGO-OVAR 2.29 |
| Fazė | III |
| Indikacija | Ligos progresavimas po ≤ 3 gydymo eilių. |
| Intervencija | Atezolizumab/Bevacizumab |
| Komanda | PI - B. Brasiūnienė. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Vyksta duomenų apdorojimas |
| Tyrimo pabaiga | 2024 m. |
| Įtraukimą Vykdantis | Ne |
| Grupė | Kiaušidžių/kiaušintakių vėžys |
| Tyrimo pavadinimas, protokolo nr. | 3 fazės, daugiacentris, arvirasis, atsitiktinių imčių tyrimas, kuriuo nemvaleukinas alfa derinyje su pembrolizumabu lyginamas su tyrėjo parinkta chemoterapija pacientėms, sergančioms platinai atspariu epiteliniu kiaušidžių, kiaušintakių ar pirminiu pilvaplėvės vėžiu (ARTISTRY-7). Protokolo Nr. ARTISTRY-7 / ALKS 4230-007 |
| Fazė | III |
| Indikacija | Platinai atsparus, ne > 5 ankstesnių gydymo eilių |
| Intervencija | Nemvaleukin+Pembro vs chemoterapija |
| Komanda | PI- B. Brasiūnienė. Koordinatoriai - A. Šukštienė, N. Kravčenko |
| Tyrimo būsena / Liko vietų | Vyksta duomenų apdorojimas |
| Tyrimo pabaiga | 2027 m. |
| Įtraukimą Vykdantis | Ne |
| Grupė | Krūties vėžys |
| Tyrimo pavadinimas, protokolo nr. | II fazės, daugiacentris, atsitiktinių imčių, atvirasis tyrimas ribociklibo 400 mg dozės derinio su nesteroidiniais aromatazės inhibitoriais saugumui ir veiksmingumui įvertinti, skiriant progresavusiu hormonų receptoriams teigiamu ir HER2 neigiamu krūties vėžiu sergančioms moterims iki ir po menopauzės, anksčiau negydytoms nuo progresavusios ligos. Protokolo Nr. CLEE011A2207 |
| Fazė | III |
| Indikacija | Histologiškai patvirtintas ER ir/ar PR teigiamas, HER2 neigiamas krūties vėžys. Yra matuojamų darinių pagal RECIST 1.1. |
| Intervencija | Ribociklibas |
| Komanda | PI- L. Daukantienė. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Vyksta duomenų apdorojimas |
| Tyrimo pabaiga | 2026 m. |
| Įtraukimą Vykdantis | Ne |
| Grupė | Nesmulkialąstelinis plaučių vėžys |
| Tyrimo pavadinimas, protokolo nr. | Neintervencinis, daugiacentris, kelių kohortų tyrimas, skirtas įvertinti atezolizumabo vartojimo išeitis ir saugumą realioje aplinkoje pacientams, kuriems gydymas skiriamas įprastinės klinikinės praktikos sąlygomis. Protokolo Nr. MO40653 |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Neintervencinis, stebimasis |
| Intervencija | Atezolizumabas |
| Komanda | PI- S. Cicėnas. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Vyksta duomenų apdorojimas |
| Tyrimo pabaiga | 2024-12-31 |
| Įtraukimą Vykdantis | Ne |
| Grupė | Plaučių vėžys |
| Tyrimo pavadinimas, protokolo nr. | Vaistų poveikio plaučių vėžiu sergančių pacientų kietajame naviko audinyje ex vivo tyrimas. Bandomasis tyrimas. Protokolo Nr. AC2101 |
| Fazė | III |
| Indikacija | Plaučių Ca, kurį planuojama operuoti |
| Intervencija | Naviko mėginio siuntimas |
| Komanda | PI- S. Cicėnas. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Vyksta duomenų apdorojimas |
| Tyrimo pabaiga | 2024-12-31 |
| Įtraukimą Vykdantis | Ne |
| Grupė | Prostatos vėžys |
| Tyrimo pavadinimas, protokolo nr. | Atviras, ne atsitiktinių imčių, I fazės, daugiacentris tyrimas, skirtas įvertinti radžio-223 biologinį pasiskirstymą tiriamiesiems, sergantiems į kaulus metastazavusiu kastracijai atspariu prostatos vėžiu (KAPV) ir gydomiems radžio-223 dichloridu. Protokolo Nr. BAY 88-8223/20511 |
| Fazė | I |
| Indikacija | Kaulų metastazės, kastracijai atspariaus prostatos vėžio (mKAPV), progresuojančiu po vieno NAH kurso |
| Intervencija | Radium-223 dichloridas |
| Komanda | PI- A. Ulys. Koordinatorius - I. Babaitienė |
| Tyrimo būsena / Liko vietų | Vyksta duomenų apdorojimas |
| Tyrimo pabaiga | 2025 m. |
| Įtraukimą Vykdantis | Ne |
| Grupė | Skrandžio ir stemplės adenokarcinoma |
| Tyrimo pavadinimas, protokolo nr. | III fazės, atsitiktinių imčių, dvigubai koduotas, klinikinis pembrolizumabo (MK 3475) kartu su chemoterapija (XP arba FP), lyginant su placebu kartu su chemoterapija (XP arba FP), tyrimas, skiriant neoadjuvantiniam / adjuvantiniam gydymui tiriamiesiems, sergantiems skrandžio ir gastroezofaginės jungties adenokarcinoma (KEYNOTE-585/). Protokolo Nr. MK-3475-585 |
| Fazė | III |
| Indikacija | Skrandžio arba GEJ adenokarcinoma ≥T3 arba N+ |
| Intervencija | Pembrolizumab + XP ar FP/ Placebas + XP ar FP |
| Komanda | PI - E. Baltruškevičienė. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Vyksta duomenų apdorojimas |
| Tyrimo pabaiga | 2024-12-31 |
| Įtraukimą Vykdantis | Ne |
| Grupė | Kiti solidiniai navikai |
| Tyrimo pavadinimas, protokolo nr. | Vaistų poveikio pleuros išskyroms ir ascitui tyrimas: bandomasis tyrimas. Protokoo Nr. AC1804 |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Pleuritas arba ascitas, kurį reikia punktuoti |
| Intervencija | Punkcija, kai eksudato > kaip 200 ml. |
| Komanda | PI- S. Cicėnas. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Vyksta duomenų apdorojimas |
| Tyrimo pabaiga | 2024-12 |
| Įtraukimą Vykdantis | Ne |
| Grupė | Tiesiosios žarnos vėžys |
| Tyrimo pavadinimas, protokolo nr. | Retrospektyvus tikrojo pasaulio totalinės neoadjuvantinės tiesiosios žarnos vėžio terapijos tyrimas. Protokolo Nr. TNT |
| Fazė | III |
| Indikacija | Nustatytas ir morfologiškai patvirtintas II-III stadijos tiesiosios žarnos vėžys |
| Intervencija | Neintervencinis, stebimasis |
| Komanda | PI- A. Dulskas. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Vyksta duomenų apdorojimas |
| Tyrimo pabaiga | 2024-12-31 |
| Įtraukimą Vykdantis | Ne |
| Grupė | Skrandžio, gastroezofaginės jungties ir stemplės adenokarcinoma |
| Tyrimo pavadinimas, protokolo nr. | Randomizuotas, atviras, daugiacentris 3 fazės domvanalimabo, zimberelimabo ir chemoterapijos tyrimas lyginant su nivolumabu ir chemoterapija, skiriant dalyviams, anksčiau negydytiems lokaliai pažengusia, neoperuotina arba metastazine skrandžio, gastroezofaginės jungties ir stemplės adenokarcinoma. Protokolo Nr. STAR-221 |
| Fazė | III |
| Indikacija | I eilė, HER2(-) matuojama liga pagal RECIST |
| Intervencija | Imunoterapija + FOLFOX6/XELOX |
| Komanda | PI- E. Baltruškevičienė. Koordinatoriai - N. Kravčenko, A. Šukštienė |
| Tyrimo būsena / Liko vietų | Gydymas |
| Tyrimo pabaiga | 2027 m. |
| Įtraukimą Vykdantis | Ne |
| Grupė | Skrandžio vėžys |
| Tyrimo pavadinimas, protokolo nr. | 2 fazės daugiacentris kelių šakų tyrimas MK 1308A (bendrai suformuluotam kvavonlimabui (MK 1308) / pembrolizumabui) įvertinti lyginant su kitomis gydymo priemonėmis dalyviams, kuriems nustatytas didelis mikrosatelitų nestabilumas (MSI-H) arba sergantiems klaidingų porų reparacijos stokos (dMMR) IV stadijos kolorektaliniu vėžiu. Protokolo nr. MK-1308A-008 |
| Fazė | II |
| Indikacija | I eilė, MSI-H |
| Intervencija | MK-1308/pembrolizumab, imunoterapija |
| Komanda | PI-E. Baltruškevičienė. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Gydymas |
| Tyrimo pabaiga | 2025 m. |
| Įtraukimą Vykdantis | Ne |
| Grupė | Kiti solidiniai navikai |
| Tyrimo pavadinimas, protokolo nr. | 1b/ 2 fazės TAK-981 ir pembrolizumabo derinio tyrimas, skirtas įvertinti derinio saugumą, toleravimą ir priešvėžinį poveikį tiriamiesiems asmenims, kuriems nustatyti tam tikri išplitę ar metastazavę solidiniai navikai. Protokolo Nr. TAK-981-1502 |
| Fazė | I/II |
| Indikacija | Imunoterapija negydytas metastazavęs gimdos kaklelio vėžys, kai liga progresuoja po 1 eilės standartinio gydymo. Neoperuojama III arba IV stadijos odos melanoma. |
| Intervencija | TAK981/Pembrolizumab |
| Komanda | PI- E. Baltruškevičienė. Koordinatoriai - N. Kravčenko, A. Šukštienė |
| Tyrimo būsena / Liko vietų | Gydymas |
| Tyrimo pabaiga | 2026 m. |
| Įtraukimą Vykdantis | Ne |
| Grupė | Prostatos vėžys |
| Tyrimo pavadinimas, protokolo nr. | Atviras, daugiacentris, vienos grupės tyrimas, kuriuo siekiama įvertinti šešių mėnesių farmacinės formos triptorelino, leidžiamo po oda, veiksmingumą ir saugumą, jį skiriant dalyviams, sergantiems lokaliai išplitusiu ir (arba) metastazavusiu prostatos vėžiu, anksčiau gydytiems ir kastruotiems GnRH analogu. PAREXEL 269263. Protokolo Nr. D-FR-52014-245 |
| Fazė | III |
| Indikacija | Gydymas GnRH analogu mažiausiai 18 mėnesių, iš kurių prieš atranką skirtas mažiausiai 3 mėn. gydymas GnRH. |
| Intervencija | Triptorelin |
| Komanda | PI- A. Ulys. Koordinatorius - I. Babaitienė |
| Tyrimo būsena / Liko vietų | Gydymas |
| Tyrimo pabaiga | 2024-12-31 |
| Įtraukimą Vykdantis | Ne |
| Grupė | SLPV |
| Tyrimo pavadinimas, protokolo nr. | 3 fazės, atsitiktinių imčių, dvigubai koduotas klinikinis tyrimas MK-7684A vartojamo derinyje su etopozidu ir platina, po to skiriant MK7684A lyginant su atezolizumabu vartojamu derinyje su etopozidu ir platina, po to skiriant atezolizumabą pirmos eilės gydymui tiriamiesiems, kuriems diagnozuotas išplitusios stadijos smulkių ląstelių plaučių vėžys. Protokolo Nr. MK-7684A-008 |
| Fazė | III |
| Indikacija | Etopozidu ir platina. Vertinama liga pagal RECIST 1.1, I-os eilės terapija |
| Intervencija | MK-7684A/ Atezolizumab |
| Komanda | PI- S. Cicėnas. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Gydymas |
| Tyrimo pabaiga | 2027-11 |
| Įtraukimą Vykdantis | Ne |
| Grupė | Skrandžio arba gastroezofaginės jungties adenokarcinoma |
| Tyrimo pavadinimas, protokolo nr. | Atsitiktinių imčių, daugiacentris, dvigubai koduotas placebu kontroliuojamas 3 fazės tyrimas, skirtas palyginti bemarituzumabą, vartojamą kartu su chemoterapija, su placebu, vartojamu su chemoterapija anksčiau negydytiems, išplitusiu skrandžio ar skrandžio ir stemplės jungties vėžiu su didele FGFR2b raiška sergantiems pacientams. ProtokoLo Nr. 20210096 |
| Fazė | III |
| Indikacija | Nustatyta padidėjusi FGFR2b raiška, nėra kontraindikacijų gydymui FOLFOX6. Matuojama liga arba nematuojama bt vertinama liga pagal RECIST 1.1 |
| Intervencija | Bemarituzumab |
| Komanda | PI- N. Lachej. Koordinatorius- A. Šukštienė |
| Tyrimo būsena / Liko vietų | Stebėjimas |
| Tyrimo pabaiga | 2025 m. |
| Įtraukimą Vykdantis | Ne |
| Grupė | Prostatos vėžys |
| Tyrimo pavadinimas, protokolo nr. | Randomizuotas, dvigubai koduotas, placebu kontroliuojamas, 3 fazės darolutamido tyrimas, skirtas kartu su androgenų deprivacijos terapija (ADT), lyginant su placebu ir ADT vyrams, sergantiems metastazavusiu, hormonams jautriu prostatos vėžiu (mHSPC). Protokolo Nr. BAY 1841788/21140 |
| Fazė | III |
| Indikacija | Prostatos vėžys (mHSPC) |
| Intervencija | Placebas ir ADT Dalorutamidas |
| Komanda | PI- A. Ulys. Koordinatorius - I. Babaitienė |
| Tyrimo būsena / Liko vietų | Gydymas |
| Tyrimo pabaiga | 2025 m. |
| Įtraukimą Vykdantis | Ne |
| Grupė | Plaučių vėžys |
| Tyrimo pavadinimas, protokolo nr. | MK-7339-013 |
| Fazė | III |
| Indikacija | SLPV, I-III st. |
| Intervencija | Pembro + ChRT, po to pembro + olaparib |
| Komanda | PI- S. Cicėnas. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Gydymas |
| Tyrimo pabaiga | 2027-12-02 |
| Įtraukimą Vykdantis | Ne |
| Grupė | Plaučių vėžys |
| Tyrimo pavadinimas, protokolo nr. | Durvalumabas (MEDI4736) po chemo-radioterapinio gydymo (DART) nesmulkialąsteliniu plaučių vėžiu (NSCLC) sergantiems pacientams – II fazės taikomasis ir biologinių žymenų tyrimas, tiriantis pacientus, kuriems rastas arba nerastas PD-L1. Protokolo Nr. DART (19-14434) |
| Fazė | II |
| Indikacija | NSCLC, biožymenų |
| Intervencija | Durvalumab |
| Komanda | PI- S. Cicėnas. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Gydymas |
| Tyrimo pabaiga | 2030 m. |
| Įtraukimą Vykdantis | Ne |
| Grupė | Krūties vėžys |
| Tyrimo pavadinimas, protokolo nr. | Individualiai pritaikyta pažasties operacija su pažasties limfmazgių disekcija arba be jos, po kurios taikoma spindulinė terapija pacientams, kuriems diagnozuotas krūties vėžys su kliniškai pakenktais limfmazgiais. Daugiacentris, atsitiktinių imčių III fazės tyrimas. Protokolo Nr. TAXIS |
| Fazė | III |
| Indikacija | KV su kliniškai pakenktais lm |
| Intervencija | Operacija su pažasties lm disekcija arba be jos, po kurios taikoma spindulinė terapija |
| Komanda | PI- V. Ostapenko. Koordinatorius - S. Činčikienė |
| Tyrimo būsena / Liko vietų | Gydymas |
| Tyrimo pabaiga | 2043 m. |
| Įtraukimą Vykdantis | Ne |
| Grupė | Nesmulkialąstelinis plaučių vėžys |
| Tyrimo pavadinimas, protokolo nr. | Nesmulkialąstelinio plaučių vėžio su EGFR mutacija pirmos eilės gydymas osimertinibu, kartu atliekant plataus masto taikomuosius tyrimus“ Protokolo Nr. FIOL |
| Fazė | II |
| Indikacija | IIIB/IV stadijos NSLPV, Išmatuojama liga pagal RECIST 1.1 |
| Intervencija | Osimertinibas |
| Komanda | PI- S. Cicėnas. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Gydymas |
| Tyrimo pabaiga | 2024-12 |
| Įtraukimą Vykdantis | Ne |
| Grupė | Nesmulkialąstelinis plaučių ir skrandžio vėžys |
| Tyrimo pavadinimas, protokolo nr. | III fazės, atsitiktinių imčių, dvigubai koduotas, klinikinis pembrolizumabo (MK 3475) kartu su chemoterapija (XP arba FP), lyginant su placebu kartu su chemoterapija (XP arba FP), tyrimas, skiriant neoadjuvantiniam / adjuvantiniam gydymui tiriamiesiems, sergantiems skrandžio ir gastroezofaginės jungties adenokarcinoma (KEYNOTE-585/) Protokolo Nr. MK-3475-587 |
| Fazė | III |
| Indikacija | Skrandžio arba GEJ adenokarcinoma |
| Intervencija | MK-3475 |
| Komanda | PI- N. Lachej. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Stebėjimas |
| Tyrimo pabaiga | 2028 m. |
| Įtraukimą Vykdantis | Ne |
| Grupė | Nesmulkialąstelinis plaučių vėžys |
| Tyrimo pavadinimas, protokolo nr. | Daugiacentris neintervencinis kohortų tyrimas, skirtas realiomis klinikinėmis sąlygomis įvertinti alk-teigiamu išplitusiu nslpv sergančių pacientų gydymą alektinibu ir gydymo išeitis (realec). Protokolo Nr. MO42122 |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Neintervencinis, stebimasis |
| Intervencija | Alektinibas |
| Komanda | PI- S. Cicėnas. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Stebėjimas |
| Tyrimo pabaiga | 2027-12 |
| Įtraukimą Vykdantis | Ne |
| Grupė | Gimdos kūno vėžys |
| Tyrimo pavadinimas, protokolo nr. | Randomizuotas, daugiacentris, dvigubai koduotas, placebu kontroliuojamas III fazės pirmosios eilės karboplatinos ir paklitakselio tyrimas kartu su durvalumabu, po kurio taikomas palaikomasis durvalumabo vartojimas kartu su olaparibu arba be jo pacientėms, kurioms naujai diagnozuotas progresavęs ar pasikartojantis gimdos kūno vėžys (DUO-E) Pr. Nr. D9311C00001 |
| Fazė | III |
| Indikacija | Naujai diagnozuotas III / IV stadijos arba pasikartojantis gimdos kūno vėžys Matuojami dariniai pagal RECIST 1.1 Netaikytas pirmosios eilės sisteminis priešvėžinis gydymas |
| Intervencija | Carbo/Pacli/ Durvalumab/Olaparib |
| Komanda | PI- B. Brasiūnienė. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Stebėjimas |
| Tyrimo pabaiga | 2025-03 |
| Įtraukimą Vykdantis | Ne |
| Grupė | Prostatos vėžys |
| Tyrimo pavadinimas, protokolo nr. | fazės atsitiktinių imčių atviras daugiacentris standartinės radžio-223 dichlorido dozės veiksmingumo ir saugumo tyrimas, palyginti su standartinėmis naujojo antihormoninio (NAH) gydymo dozėmis, pacientams, sergantiems į kaulus išplitusiu metastaziniu kastracijai atspariu prostatos vėžiu (mKAPV), progresuojančiu po vieno NAH kurso. Protokolo Nr. BAY 88-8223/20510 |
| Fazė | IV |
| Indikacija | Metastazavęs vėžys po 1-2 gydymo eilių. Taikomas gydymas kauklus stiprinančiais vaistais bent 6 mėn. |
| Intervencija | Radium-223/NAH |
| Komanda | PI-A. Ulys. Koordinatorius - I. Babaitienė |
| Tyrimo būsena / Liko vietų | Stebėjimas |
| Tyrimo pabaiga | 2025 m. |
| Įtraukimą Vykdantis | Ne |
| Grupė | Nesmulkialąstelinis plaučių vėžys |
| Tyrimo pavadinimas, protokolo nr. | III fazės, atsitiktinių imčių, dvigubai koduotas, platinos dupletų chemoterapijos kartu su arba be pembrolizumabo (MK-3475) tyrimas, skiriant neoadjuvantiniam / adjuvantiniam gydymui tiriamiesiems, sergantiems rezektabiliu II, IIIA ir IIIB (T3-4N2) stadijų nesmulkialąsteliniu plaučių vėžiu (NSPV) (KEYNOTE-671). Protokolo Nr. MK-3475-671 |
| Fazė | III |
| Indikacija | NSPV |
| Intervencija | Pembrolizumab |
| Komanda | PI-S. Cicėnas. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Stebėjimas |
| Tyrimo pabaiga | 2026-07-29 |
| Įtraukimą Vykdantis | Ne |
| Grupė | Kiti solidiniai navikai |
| Tyrimo pavadinimas, protokolo nr. | Vėžiu sergančių pacientų atranka siekiant efektyvaus patekimo į klinikinius tyrimus. Protokolo Nr. EORTC-1553 (SPECTA) |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Galvos kaklo, NSLPV, storosios žarnos Ca, krūties Ca, inkstų Ca. Kraujo mėginių rinkimas |
| Intervencija | Neintervencinis, biožymenų |
| Komanda | PI- B. Brasiūnienė. Koordinatoriai - N. Kravčenko A. Šukštienė, V. Kūgis |
| Tyrimo būsena / Liko vietų | Stebėjimas |
| Tyrimo pabaiga | 2024-12 |
| Įtraukimą Vykdantis | Ne |
| Grupė | Smulkialąstelinis plaučių vėžys |
| Tyrimo pavadinimas, protokolo nr. | Atsitiktinių imčių, II fazės tyrimas, skirtas palyginti gydymą atezolizumabu po chemospindulinio gydymo vietiškai išplitusio smulkialąstelinio plaučių vėžio atveju su chemospinduliniu gydymu neskiriant atezolizumabo. Protokolo Nr. MO40379 ACHILES 2017-12 |
| Fazė | II |
| Indikacija | plaučių vėžys su chemospinduliniu gydymu |
| Intervencija | Atezolizumabas po ChRT |
| Komanda | PI- S. Cicėnas. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | Stebėjimas |
| Tyrimo pabaiga | 2026-12 |
| Įtraukimą Vykdantis | Ne |
| Grupė | Tyrimo pavadinimas, protokolo nr. | Fazė | Indikacija | Intervencija | Komanda | Tyrimo būsena / Liko vietų | Tyrimo pabaiga | Įtraukimą Vykdantis | |
| Melanoma | Atsitiktinių imčių, lygiagrečių grupių tyrimas, skirtas palyginti GME75. Protokolo Nr. CGME751A12101 | I | IIB, IIC, III st. melanoma, 2-13 sav. po rezekcijos | GME751/Pembrolizumab | PI-V. Urbonas. Koordinatoriai- A. Šukštienė, I.R. Kasiliauskaitė | 8 | 2025-06 | Taip | |
| Melanoma | Atsitiktinių imčių dvigubai aklas tyrimas, kuriame vertinamas ABP 206 farmakokinetinis panašumas, palyginti su OPDIVO® (nivolumabu), gydant III ar IV stadijos melanomos pacientus, kuriems taikoma adjuvantinė terapija. Protokolo Nr. 20220083 | III | Adjuvantas, kai radikaliai rezekuota III arba IV stadija | Nivolumabas vs biosimiliarus Nivolumabas | PI-V. Urbonas, Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė | Gydymas | 2024-10-11 | Ne | |
| Melanoma | Atviras I fazės daugiacentris, randomizuotas, dvigubai aklas tyrimas, kuriame vertinamas ABP 206 farmakokinetinis panašumas, palyginti su OPDIVO® (Nivolumabu), skirto III ar IV stadijos melanomai, sergantiems rezekuotomis melanomomis adjuvantinėje aplinkoje. Protokolo Nr. NECVAX-NEO1-LT |
I | Bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST | Papildoma geriamoji vakcina | PI-V. Urbonas. Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė | 6 | 2026-11 | Taip | |
| Melanoma | Epigenetiniai kraujyje laisvai cirkuliuojančios DNR žymenys ankstyvajai vėžio atkryčio diagnostikai. Protokolo Nr. EpiCancer2023 | Biomedicininis tyrimas | Planuojama perioperacinė chemoterapija | Kraujo ėminiai cfDNR nustatyti | PI - A. Dulskas, Koordinatorius - N. Kravčenko | 20 | 2028 m. | Taip | |
| Kiaušidžių vėžys | Atsitiktinių imčių klinikinis tyrimas palaikomajai terapijai olaparibu, durvalumabu, NSGO-CTU-DOVACC. Protokolo Nr. NSGO-CTU-DOVACC | III | Platinai jautrus, I arba II atkrytis, BRCA (-) | Palaikomasis gydymas olaparibu+/-durvaliumabu+/-UV1 | PI- B. Brasiūnienė; Koordinatorius A. Šukštienė | 3 | 2026-12 | Taip | |
| Melanoma | Atsitiktinių imčių dvigubai aklas tyrimas, kuriame vertinamas ABP 206 veiksmingumas, saugumas ir imunogeniškumas, palyginti su OPDIVO® (nivolumabu) gydymui nepasirengusiems asmenims, sergantiems neišplitusia ar metastazavusia melanoma. Protokolo Nr. 20210031 | III | I eilė, kai nerezektabili III / IV st | Nivolumabas vs biosimiliarus Nivolumabas | PI-V. Urbonas. Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė | 6 | 2025-01 | Taip | |
| Krūties vėžys | CHAIMELEON dirbtinio intelekto įrankių perkėlimo iš laboratorijos į rinką spartinimas vėžio valdymui. Protokolo Nr. CHAIMELEON | Biomedicininis tyrimas | Krūties Ca | Radiologinių vaizdų ir klinik. duomenų surinkimas | PI-J. Ušinskienė; Koordinatorius - I.R.Kasiliauskaitė | 995 | 2025 | Taip | |
| Krūties vėžys | Atsitiktinių imčių III fazės tyrimas, pažasties operacija su pažasties limfmazgių, TAXIS | III | Krūties Ca su kliniškai pakenktais lm | Operacija su pažasties lm disekcija arba be jos, po kurios taikoma spindulinė terapija | PI- V. Ostapenko; Koordinatorius A. Šukštienė | 44 | 2024-12 | Taip | |
| Krūties vėžys | Pažasties limfmazgių disekcijos sąsaja su onkologiniu saugumu pacientams. Protokolo Nr. OPBC-07/microNAC | III | Krūties Ca, kai nustatoma likusių mikrometastazių po neoadjuvantinės chemoterapijos, kai taikyta pažasties disekacija arba be jos. | Duomenų rinkimas | PI- V. Ostapenko; Koordinatorius I. R. Kasiliauskaitė | 24 | 2024-12 | Taip | |
| Skrandžio vėžys | PIPAC | Pilotinis | I eilė, HER2(-), metastazes tik pilvaplėvėje | PIPAC + FOLFOX | PI – A. Baušys, Koordinatorius A. Šukštienė | 15 | 2024 m. | Taip | |
| Skrandžio vėžys | Epigenetiniai kraujyje laisvai cirkuliuojančios DNR žymenys ankstyvajai vėžio atkryčio diagnostikai. Protokolo Nr. EpiCancer2023 | Biomedicininis tyrimas | Planuojama perioperacinė chemoterapija | Kraujo ėminiai cfDNR nustatyti | PI- A. Dulskas. Koordinatorius N. Kravčenko | 20 | 2028 m. | Taip | |
| Storosios žarnos ir plonosios žarnos vėžys | Epigenetiniai kraujyje laisvai cirkuliuojančios DNR žymenys ankstyvajai vėžio atkryčio diagnostikai. Protokolo Nr. EpiCancer2023. | Biomedicininis tyrimas | Planuojama neoadjuvantinė chemoterapija | Kraujo ėminiai cfDNR nustatyti | PI - A. Dulskas. Koordinatorius N. Kravčenko | 20 | 2028 m. | Taip | |
| Storosios žarnos ir plonosios žarnos vėžys | CHAIMELEON dirbtinio intelekto įrankių perkėlimo iš laboratorijos į rinką spartinimas vėžio valdymui. Protokolo Nr. CHAIMELEON | Biomedicininis tyrimas | Storosios žarnos ir plonosios žarnos vėžio Ca | Radiologinių vaizdų ir klinik. duomenų surinkimas | PI-J. Ušinskienė. Koordinatorius - I.R.Kasiliauskaitė | 995 | 2025 m. | Taip | |
| Galvos kaklo vėžys | Atviras I fazės daugiacentris, randomizuotas, dvigubai aklas tyrimas, kuriame vertinamas ABP 206 farmakokinetinis panašumas, palyginti su OPDIVO® (Nivolumabu), skirto III ar IV stadijos melanomai, sergantiems rezekuotomis melanomomis adjuvantinėje aplinkoje. Protokolo Nr. NECVAX-NEO1-LT |
I | Bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST | Papildoma geriamoji vakcina | PI-V. Urbonas; Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė | 6 | 2026-11 | Taip | |
| Prostatos vėžys | CHAIMELEON dirbtinio intelekto įrankių perkėlimo iš laboratorijos į rinką spartinimas vėžio valdymui. Protokolo Nr. CHAIMELEON | Biomedicininis tyrimas | Prostatos Ca | Radiologinių vaizdų ir klinik. duomenų surinkimas | PI-J. Ušinskienė. Koordinatorius - I.R.Kasiliauskaitė | 995 | 2025 | Taip | |
| Prostatos vėžys | 3 fazės, atsitiktinių imčių, atviras MK-5684 ir alternatyvaus preparato abiraterono acetato arba enzalutamido tyrimas, skirtas tiriamiesiems, sergantiems metastazavusiu, kastracijai atspariu prostatos vėžiu (mKAPV), progresavusiu po ankstesnio gydymo vienu naujos kartos hormoniniu preparatu (NKHP) Protokolo Nr. MK5684-004 | III | Kastracijai atsparus prostatos vėžys (mKAPV), progresavęs po ankstesnio gydymo vienu naujos kartos hormoniniu preparatu (NKHP) | MK-5684, abiraterono acetatas arba enzalutamidas | PI - A. Ulys. Koordinatorius - A. Šukštienė | 9 | 2026 m. | Taip | |
| Inkstų vėžys | Atviras I fazės daugiacentris, randomizuotas, dvigubai aklas tyrimas, kuriame vertinamas ABP 206 farmakokinetinis panašumas, palyginti su OPDIVO® (Nivolumabu), skirto III ar IV stadijos melanomai, sergantiems rezekuotomis melanomomis adjuvantinėje aplinkoje. Protokolo Nr. NECVAX-NEO1-LT |
I | Bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST | Papildoma geriamoji vakcina | PI-V. Urbonas; Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė | 6 | 2026-11 | Taip | |
| Plaučių vėžys | 3 fazės, atsitiktinių imčių, dvigubai koduotas, placebu ir aktyviuoju palyginamuoju preparatu kontroliuojamas klinikinis tyrimas, skirtas palyginti adjuvanto V940 (mRNR-4157) skyrimą kartu su pembrolizumabu ir adjuvanto placebo skyrimą kartu su pembrolizumabu dalyviams, sergantiems rezekuotu II, IIIA, IIIB (N2) stadijos nesmulkiųjų ląstelių plaučių vėžiu. Protokolo Nr. V940-002 | III | NSLPV, išoperuotas (R0) II, IIIA, IIIB st, N2, I eilė | V940 + Pembro | PI- V. Gedvilaitė. Koordinatorius - A. Šukštienė | 4 | 2025 m. | Taip | |
| Plaučių vėžys | Atviras I fazės daugiacentris, randomizuotas, dvigubai aklas tyrimas, kuriame vertinamas ABP 206 farmakokinetinis panašumas, palyginti su OPDIVO® (Nivolumabu), skirto III ar IV stadijos melanomai, sergantiems rezekuotomis melanomomis adjuvantinėje aplinkoje. Protokolo Nr. NECVAX-NEO1-LT Protokolo Nr. NECVAX-NEO1-LT |
I | NSCLC bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST | Papildoma geriamoji vakcina | PI-V. Urbonas; Sub-I - E. Baltruškevičienė, L. Gatijatullin; Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė | 6 | 2026-11 | Taip | |
| Plaučių vėžys | CHAIMELEON dirbtinio intelekto įrankių perkėlimo iš laboratorijos į rinką spartinimas vėžio valdymui. Protokolo Nr. CHAIMELEON | Biomedicininis tyrimas | Plaučių Ca | Radiologinių vaizdų ir klinik. duomenų surinkimas | PI-J. Ušinskienė. Koordinatorius - I. R. Kasiliauskaitė | 995 | 2025 m. | Taip | |
| Plaučių vėžys | Atviras, daugiacentris, 3 fazės atsitiktinių imčių, aktyviais lyginamaisiais metodais kontroliuojamas klinikinis tyrimas Pembrolizumabo (MK-3475) derinyje su Sacituzumab Govitecan, palyginti su MK-3475 monoterapija, kaip pirmos eilės gydymu sergant PD L1 TPS didesnis arba lygus 50 % metastazavusiu nesmulkialąsteliniu plaučių vėžiu (KEYNOTE D46/EVOKE-03). Protokolo Nr. MK-3475-D46 |
III | NSLPV, IV st, PD-L1>50%, I eilė | Pembro+sacituzumab govitekan | PI – S. Cicėnas. Koordinatoriai - A. Šukštienė, I. R. Kasiliauskaitė | 5 | 2025-03 | Taip | |
| Kiti solidiniai navikai | Atvirasis, I fazės daugiacentris, klinikinis tyrimas siekiant įvertinti NECVAX-NEO1, Protokolo Nr. NECVAX-NEO1-LT | I | Bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST | Papildoma geriamoji vakcina | PI-V. Urbonas; Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė | 6 | 2026-11 | Taip | |
| Kiti solidiniai navikai | Europos onkologinio gyvenimo kokybės priemonių rinkinio patvirtinimas. Europos pilotinė apklausa. Protokolo Nr. EUonQoL | Biomedicininis tyrimas | Kiti solidiniai navikai - aktyvus gydymas, stebėsena arba paliatyvus gydymas | Neintervencinis, stebimasis | PI- A. Dulskas; Koordinatoriai N. Kravčenko, I. R. Kasiliauskaitė | 79 | 2024-11 | Taip | |
| Gimdos kūno vėžys | II/III fazės navtemadlino kaip palaikomojo gydymo tyrimas pacientėms, sergančioms laukinio tipo TP53 (TP53WT) pažengusiu ar atsinaujinusiu endometriumo vėžiu, kurios reagavo į chemoterapiją. Protokolo Nr. KRT-232-118 | II/III | TP53WT, pirminė išplitusi liga arba atkrytis, Pravesti iki 6 ciklų TP chemoterapijos ir pasiektas CR arba PR pagal RECIST | Palaikomasis gydymas navtemadlinu | PI- B. Brasiūnienė. Koordinatoriai N. Kravčenko, A. Šukštienė | Vyksta duomenų apdorojimas | Sustabdytas tyrimas 2024-07-29 | Ne | |
| Gimdos gleivinės vėžys | Gimdos gleivinės (endometriumo) vėžio nustatymas taikant gimdos kaklelio DNR metilinimo tyrimus. Protokolo Nr. Endo-cancer-2022 | Biomedicininis tyrimas | Biožymenų | Gimdos gleivinės vėžio pacientų mėginių rinkimas. Suplanuota, bet dar neįvykusi visiška histerektomija | PI- R. Čiurlienė. Koordinatorius - A. Šukštienė | Vyksta duomenų apdorojimas | 2025 m. | Ne | |
| Kiaušidžių vėžys | Chemoimunoterapijos, taikant autologinius dendritinių ląstelių preparatus, saugumo tyrimas, gydant pacientes, sergančias 3 stadijos kiaušidžių vėžiu. Protokolo Nr. ChImDLP-2 | I/II | Atlikta optimali citoredukcija (R0). Indikuotina pooperacinė chemoterapija karboplatinos ir paklitakselio deriniu. | Dendritinių ląstelių preparatas (DLP) | PI-B. Intaitė. Koordinatorius - A. Šukštienė | Tyrimas sustabdytas. Vyksta duomenų apdorojimas | 2026 m. | Ne | |
| Kiaušidžių vėžys | Atezolizumabo derinys su bevacizumabu ir chemoterapija, lyginant su bevacizumabu ir chemoterapija, atsinaujinus kiaušidžių vėžiui – atsitiktinių imčių, III fazės tyrimas. Protokolo Nr. AGO-OVAR 2.29 | III | Ligos progresavimas po ≤ 3 gydymo eilių. | Atezolizumab/Bevacizumab | PI - B. Brasiūnienė. Koordinatorius - A. Šukštienė | Vyksta duomenų apdorojimas | 2024 m. | Ne | |
| Kiaušidžių/kiaušintakių vėžys | 3 fazės, daugiacentris, arvirasis, atsitiktinių imčių tyrimas, kuriuo nemvaleukinas alfa derinyje su pembrolizumabu lyginamas su tyrėjo parinkta chemoterapija pacientėms, sergančioms platinai atspariu epiteliniu kiaušidžių, kiaušintakių ar pirminiu pilvaplėvės vėžiu (ARTISTRY-7). Protokolo Nr. ARTISTRY-7 / ALKS 4230-007 | III | Platinai atsparus, ne > 5 ankstesnių gydymo eilių | Nemvaleukin+Pembro vs chemoterapija | PI- B. Brasiūnienė. Koordinatoriai - A. Šukštienė, N. Kravčenko | Vyksta duomenų apdorojimas | 2027 m. | Ne | |
| Krūties vėžys | II fazės, daugiacentris, atsitiktinių imčių, atvirasis tyrimas ribociklibo 400 mg dozės derinio su nesteroidiniais aromatazės inhibitoriais saugumui ir veiksmingumui įvertinti, skiriant progresavusiu hormonų receptoriams teigiamu ir HER2 neigiamu krūties vėžiu sergančioms moterims iki ir po menopauzės, anksčiau negydytoms nuo progresavusios ligos. Protokolo Nr. CLEE011A2207 | III | Histologiškai patvirtintas ER ir/ar PR teigiamas, HER2 neigiamas krūties vėžys. Yra matuojamų darinių pagal RECIST 1.1. | Ribociklibas | PI- L. Daukantienė. Koordinatorius - A. Šukštienė | Vyksta duomenų apdorojimas | 2026 m. | Ne | |
| Nesmulkialąstelinis plaučių vėžys | Neintervencinis, daugiacentris, kelių kohortų tyrimas, skirtas įvertinti atezolizumabo vartojimo išeitis ir saugumą realioje aplinkoje pacientams, kuriems gydymas skiriamas įprastinės klinikinės praktikos sąlygomis. Protokolo Nr. MO40653 | Biomedicininis tyrimas | Neintervencinis, stebimasis | Atezolizumabas | PI- S. Cicėnas. Koordinatorius - A. Šukštienė | Vyksta duomenų apdorojimas | 2024-12-31 | Ne | |
| Plaučių vėžys | Vaistų poveikio plaučių vėžiu sergančių pacientų kietajame naviko audinyje ex vivo tyrimas. Bandomasis tyrimas. Protokolo Nr. AC2101 | III | Plaučių Ca, kurį planuojama operuoti | Naviko mėginio siuntimas | PI- S. Cicėnas. Koordinatorius - A. Šukštienė | Vyksta duomenų apdorojimas | 2024-12-31 | Ne | |
| Prostatos vėžys | Atviras, ne atsitiktinių imčių, I fazės, daugiacentris tyrimas, skirtas įvertinti radžio-223 biologinį pasiskirstymą tiriamiesiems, sergantiems į kaulus metastazavusiu kastracijai atspariu prostatos vėžiu (KAPV) ir gydomiems radžio-223 dichloridu. Protokolo Nr. BAY 88-8223/20511 | I | Kaulų metastazės, kastracijai atspariaus prostatos vėžio (mKAPV), progresuojančiu po vieno NAH kurso | Radium-223 dichloridas | PI- A. Ulys. Koordinatorius - I. Babaitienė | Vyksta duomenų apdorojimas | 2025 m. | Ne | |
| Skrandžio ir stemplės adenokarcinoma | III fazės, atsitiktinių imčių, dvigubai koduotas, klinikinis pembrolizumabo (MK 3475) kartu su chemoterapija (XP arba FP), lyginant su placebu kartu su chemoterapija (XP arba FP), tyrimas, skiriant neoadjuvantiniam / adjuvantiniam gydymui tiriamiesiems, sergantiems skrandžio ir gastroezofaginės jungties adenokarcinoma (KEYNOTE-585/). Protokolo Nr. MK-3475-585 | III | Skrandžio arba GEJ adenokarcinoma ≥T3 arba N+ | Pembrolizumab + XP ar FP/ Placebas + XP ar FP | PI - E. Baltruškevičienė. Koordinatorius - A. Šukštienė | Vyksta duomenų apdorojimas | 2024-12-31 | Ne | |
| Kiti solidiniai navikai | Vaistų poveikio pleuros išskyroms ir ascitui tyrimas: bandomasis tyrimas. Protokoo Nr. AC1804 | Biomedicininis tyrimas | Pleuritas arba ascitas, kurį reikia punktuoti | Punkcija, kai eksudato > kaip 200 ml. | PI- S. Cicėnas. Koordinatorius - A. Šukštienė | Vyksta duomenų apdorojimas | 2024-12 | Ne | |
| Tiesiosios žarnos vėžys | Retrospektyvus tikrojo pasaulio totalinės neoadjuvantinės tiesiosios žarnos vėžio terapijos tyrimas. Protokolo Nr. TNT | III | Nustatytas ir morfologiškai patvirtintas II-III stadijos tiesiosios žarnos vėžys | Neintervencinis, stebimasis | PI- A. Dulskas. Koordinatorius - A. Šukštienė | Vyksta duomenų apdorojimas | 2024-12-31 | Ne | |
| Skrandžio, gastroezofaginės jungties ir stemplės adenokarcinoma | Randomizuotas, atviras, daugiacentris 3 fazės domvanalimabo, zimberelimabo ir chemoterapijos tyrimas lyginant su nivolumabu ir chemoterapija, skiriant dalyviams, anksčiau negydytiems lokaliai pažengusia, neoperuotina arba metastazine skrandžio, gastroezofaginės jungties ir stemplės adenokarcinoma. Protokolo Nr. STAR-221 | III | I eilė, HER2(-) matuojama liga pagal RECIST | Imunoterapija + FOLFOX6/XELOX | PI- E. Baltruškevičienė. Koordinatoriai - N. Kravčenko, A. Šukštienė | Gydymas | 2027 m. | Ne | |
| Skrandžio vėžys | 2 fazės daugiacentris kelių šakų tyrimas MK 1308A (bendrai suformuluotam kvavonlimabui (MK 1308) / pembrolizumabui) įvertinti lyginant su kitomis gydymo priemonėmis dalyviams, kuriems nustatytas didelis mikrosatelitų nestabilumas (MSI-H) arba sergantiems klaidingų porų reparacijos stokos (dMMR) IV stadijos kolorektaliniu vėžiu. Protokolo nr. MK-1308A-008 | II | I eilė, MSI-H | MK-1308/pembrolizumab, imunoterapija | PI-E. Baltruškevičienė. Koordinatorius - A. Šukštienė | Gydymas | 2025 m. | Ne | |
| Kiti solidiniai navikai | 1b/ 2 fazės TAK-981 ir pembrolizumabo derinio tyrimas, skirtas įvertinti derinio saugumą, toleravimą ir priešvėžinį poveikį tiriamiesiems asmenims, kuriems nustatyti tam tikri išplitę ar metastazavę solidiniai navikai. Protokolo Nr. TAK-981-1502 | I/II | Imunoterapija negydytas metastazavęs gimdos kaklelio vėžys, kai liga progresuoja po 1 eilės standartinio gydymo. Neoperuojama III arba IV stadijos odos melanoma. | TAK981/Pembrolizumab | PI- E. Baltruškevičienė. Koordinatoriai - N. Kravčenko, A. Šukštienė | Gydymas | 2026 m. | Ne | |
| Prostatos vėžys | Atviras, daugiacentris, vienos grupės tyrimas, kuriuo siekiama įvertinti šešių mėnesių farmacinės formos triptorelino, leidžiamo po oda, veiksmingumą ir saugumą, jį skiriant dalyviams, sergantiems lokaliai išplitusiu ir (arba) metastazavusiu prostatos vėžiu, anksčiau gydytiems ir kastruotiems GnRH analogu. PAREXEL 269263. Protokolo Nr. D-FR-52014-245 | III | Gydymas GnRH analogu mažiausiai 18 mėnesių, iš kurių prieš atranką skirtas mažiausiai 3 mėn. gydymas GnRH. | Triptorelin | PI- A. Ulys. Koordinatorius - I. Babaitienė | Gydymas | 2024-12-31 | Ne | |
| SLPV | 3 fazės, atsitiktinių imčių, dvigubai koduotas klinikinis tyrimas MK-7684A vartojamo derinyje su etopozidu ir platina, po to skiriant MK7684A lyginant su atezolizumabu vartojamu derinyje su etopozidu ir platina, po to skiriant atezolizumabą pirmos eilės gydymui tiriamiesiems, kuriems diagnozuotas išplitusios stadijos smulkių ląstelių plaučių vėžys. Protokolo Nr. MK-7684A-008 | III | Etopozidu ir platina. Vertinama liga pagal RECIST 1.1, I-os eilės terapija | MK-7684A/ Atezolizumab | PI- S. Cicėnas. Koordinatorius - A. Šukštienė | Gydymas | 2027-11 | Ne | |
| Skrandžio arba gastroezofaginės jungties adenokarcinoma | Atsitiktinių imčių, daugiacentris, dvigubai koduotas placebu kontroliuojamas 3 fazės tyrimas, skirtas palyginti bemarituzumabą, vartojamą kartu su chemoterapija, su placebu, vartojamu su chemoterapija anksčiau negydytiems, išplitusiu skrandžio ar skrandžio ir stemplės jungties vėžiu su didele FGFR2b raiška sergantiems pacientams. ProtokoLo Nr. 20210096 | III | Nustatyta padidėjusi FGFR2b raiška, nėra kontraindikacijų gydymui FOLFOX6. Matuojama liga arba nematuojama bt vertinama liga pagal RECIST 1.1 | Bemarituzumab | PI- N. Lachej. Koordinatorius- A. Šukštienė | Stebėjimas | 2025 m. | Ne | |
| Prostatos vėžys | Randomizuotas, dvigubai koduotas, placebu kontroliuojamas, 3 fazės darolutamido tyrimas, skirtas kartu su androgenų deprivacijos terapija (ADT), lyginant su placebu ir ADT vyrams, sergantiems metastazavusiu, hormonams jautriu prostatos vėžiu (mHSPC). Protokolo Nr. BAY 1841788/21140 | III | Prostatos vėžys (mHSPC) | Placebas ir ADT Dalorutamidas | PI- A. Ulys. Koordinatorius - I. Babaitienė | Gydymas | 2025 m. | Ne | |
| Plaučių vėžys | MK-7339-013 | III | SLPV, I-III st. | Pembro + ChRT, po to pembro + olaparib | PI- S. Cicėnas. Koordinatorius - A. Šukštienė | Gydymas | 2027-12-02 | Ne | |
| Plaučių vėžys | Durvalumabas (MEDI4736) po chemo-radioterapinio gydymo (DART) nesmulkialąsteliniu plaučių vėžiu (NSCLC) sergantiems pacientams – II fazės taikomasis ir biologinių žymenų tyrimas, tiriantis pacientus, kuriems rastas arba nerastas PD-L1. Protokolo Nr. DART (19-14434) | II | NSCLC, biožymenų | Durvalumab | PI- S. Cicėnas. Koordinatorius - A. Šukštienė | Gydymas | 2030 m. | Ne | |
| Krūties vėžys | Individualiai pritaikyta pažasties operacija su pažasties limfmazgių disekcija arba be jos, po kurios taikoma spindulinė terapija pacientams, kuriems diagnozuotas krūties vėžys su kliniškai pakenktais limfmazgiais. Daugiacentris, atsitiktinių imčių III fazės tyrimas. Protokolo Nr. TAXIS | III | KV su kliniškai pakenktais lm | Operacija su pažasties lm disekcija arba be jos, po kurios taikoma spindulinė terapija | PI- V. Ostapenko. Koordinatorius - S. Činčikienė | Gydymas | 2043 m. | Ne | |
| Nesmulkialąstelinis plaučių vėžys | Nesmulkialąstelinio plaučių vėžio su EGFR mutacija pirmos eilės gydymas osimertinibu, kartu atliekant plataus masto taikomuosius tyrimus“ Protokolo Nr. FIOL | II | IIIB/IV stadijos NSLPV, Išmatuojama liga pagal RECIST 1.1 | Osimertinibas | PI- S. Cicėnas. Koordinatorius - A. Šukštienė | Gydymas | 2024-12 | Ne | |
| Nesmulkialąstelinis plaučių ir skrandžio vėžys | III fazės, atsitiktinių imčių, dvigubai koduotas, klinikinis pembrolizumabo (MK 3475) kartu su chemoterapija (XP arba FP), lyginant su placebu kartu su chemoterapija (XP arba FP), tyrimas, skiriant neoadjuvantiniam / adjuvantiniam gydymui tiriamiesiems, sergantiems skrandžio ir gastroezofaginės jungties adenokarcinoma (KEYNOTE-585/) Protokolo Nr. MK-3475-587 | III | Skrandžio arba GEJ adenokarcinoma | MK-3475 | PI- N. Lachej. Koordinatorius - A. Šukštienė | Stebėjimas | 2028 m. | Ne | |
| Nesmulkialąstelinis plaučių vėžys | Daugiacentris neintervencinis kohortų tyrimas, skirtas realiomis klinikinėmis sąlygomis įvertinti alk-teigiamu išplitusiu nslpv sergančių pacientų gydymą alektinibu ir gydymo išeitis (realec). Protokolo Nr. MO42122 | Biomedicininis tyrimas | Neintervencinis, stebimasis | Alektinibas | PI- S. Cicėnas. Koordinatorius - A. Šukštienė | Stebėjimas | 2027-12 | Ne | |
| Gimdos kūno vėžys | Randomizuotas, daugiacentris, dvigubai koduotas, placebu kontroliuojamas III fazės pirmosios eilės karboplatinos ir paklitakselio tyrimas kartu su durvalumabu, po kurio taikomas palaikomasis durvalumabo vartojimas kartu su olaparibu arba be jo pacientėms, kurioms naujai diagnozuotas progresavęs ar pasikartojantis gimdos kūno vėžys (DUO-E) Pr. Nr. D9311C00001 | III | Naujai diagnozuotas III / IV stadijos arba pasikartojantis gimdos kūno vėžys Matuojami dariniai pagal RECIST 1.1 Netaikytas pirmosios eilės sisteminis priešvėžinis gydymas |
Carbo/Pacli/ Durvalumab/Olaparib | PI- B. Brasiūnienė. Koordinatorius - A. Šukštienė | Stebėjimas | 2025-03 | Ne | |
| Prostatos vėžys | fazės atsitiktinių imčių atviras daugiacentris standartinės radžio-223 dichlorido dozės veiksmingumo ir saugumo tyrimas, palyginti su standartinėmis naujojo antihormoninio (NAH) gydymo dozėmis, pacientams, sergantiems į kaulus išplitusiu metastaziniu kastracijai atspariu prostatos vėžiu (mKAPV), progresuojančiu po vieno NAH kurso. Protokolo Nr. BAY 88-8223/20510 |
IV | Metastazavęs vėžys po 1-2 gydymo eilių. Taikomas gydymas kauklus stiprinančiais vaistais bent 6 mėn. | Radium-223/NAH | PI-A. Ulys. Koordinatorius - I. Babaitienė | Stebėjimas | 2025 m. | Ne | |
| Nesmulkialąstelinis plaučių vėžys | III fazės, atsitiktinių imčių, dvigubai koduotas, platinos dupletų chemoterapijos kartu su arba be pembrolizumabo (MK-3475) tyrimas, skiriant neoadjuvantiniam / adjuvantiniam gydymui tiriamiesiems, sergantiems rezektabiliu II, IIIA ir IIIB (T3-4N2) stadijų nesmulkialąsteliniu plaučių vėžiu (NSPV) (KEYNOTE-671). Protokolo Nr. MK-3475-671 | III | NSPV | Pembrolizumab | PI-S. Cicėnas. Koordinatorius - A. Šukštienė | Stebėjimas | 2026-07-29 | Ne | |
| Kiti solidiniai navikai | Vėžiu sergančių pacientų atranka siekiant efektyvaus patekimo į klinikinius tyrimus. Protokolo Nr. EORTC-1553 (SPECTA) | Biomedicininis tyrimas | Galvos kaklo, NSLPV, storosios žarnos Ca, krūties Ca, inkstų Ca. Kraujo mėginių rinkimas | Neintervencinis, biožymenų | PI- B. Brasiūnienė. Koordinatoriai - N. Kravčenko A. Šukštienė, V. Kūgis | Stebėjimas | 2024-12 | Ne | |
| Smulkialąstelinis plaučių vėžys | Atsitiktinių imčių, II fazės tyrimas, skirtas palyginti gydymą atezolizumabu po chemospindulinio gydymo vietiškai išplitusio smulkialąstelinio plaučių vėžio atveju su chemospinduliniu gydymu neskiriant atezolizumabo. Protokolo Nr. MO40379 ACHILES 2017-12 | II | plaučių vėžys su chemospinduliniu gydymu | Atezolizumabas po ChRT | PI- S. Cicėnas. Koordinatorius - A. Šukštienė | Stebėjimas | 2026-12 | Ne |
| Grupė | Melanoma |
| Tyrimo pavadinimas, protokolo nr. | Atsitiktinių imčių, lygiagrečių grupių tyrimas, skirtas palyginti GME75. Protokolo Nr. CGME751A12101 |
| Fazė | I |
| Indikacija | IIB, IIC, III st. melanoma, 2-13 sav. po rezekcijos |
| Intervencija | GME751/Pembrolizumab |
| Komanda | PI-V. Urbonas. Koordinatoriai- A. Šukštienė, I.R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 8 |
| Tyrimo pabaiga | 2025-06 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Melanoma |
| Tyrimo pavadinimas, protokolo nr. | Atviras I fazės daugiacentris, randomizuotas, dvigubai aklas tyrimas, kuriame vertinamas ABP 206 farmakokinetinis panašumas, palyginti su OPDIVO® (Nivolumabu), skirto III ar IV stadijos melanomai, sergantiems rezekuotomis melanomomis adjuvantinėje aplinkoje. Protokolo Nr. NECVAX-NEO1-LT |
| Fazė | I |
| Indikacija | Bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST |
| Intervencija | Papildoma geriamoji vakcina |
| Komanda | PI-V. Urbonas. Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 6 |
| Tyrimo pabaiga | 2026-11 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Melanoma |
| Tyrimo pavadinimas, protokolo nr. | Epigenetiniai kraujyje laisvai cirkuliuojančios DNR žymenys ankstyvajai vėžio atkryčio diagnostikai. Protokolo Nr. EpiCancer2023 |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Planuojama perioperacinė chemoterapija |
| Intervencija | Kraujo ėminiai cfDNR nustatyti |
| Komanda | PI - A. Dulskas, Koordinatorius - N. Kravčenko |
| Tyrimo būsena / Liko vietų | 20 |
| Tyrimo pabaiga | 2028 m. |
| Įtraukimą Vykdantis | Taip |
| Grupė | Kiaušidžių vėžys |
| Tyrimo pavadinimas, protokolo nr. | Atsitiktinių imčių klinikinis tyrimas palaikomajai terapijai olaparibu, durvalumabu, NSGO-CTU-DOVACC. Protokolo Nr. NSGO-CTU-DOVACC |
| Fazė | III |
| Indikacija | Platinai jautrus, I arba II atkrytis, BRCA (-) |
| Intervencija | Palaikomasis gydymas olaparibu+/-durvaliumabu+/-UV1 |
| Komanda | PI- B. Brasiūnienė; Koordinatorius A. Šukštienė |
| Tyrimo būsena / Liko vietų | 3 |
| Tyrimo pabaiga | 2026-12 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Melanoma |
| Tyrimo pavadinimas, protokolo nr. | Atsitiktinių imčių dvigubai aklas tyrimas, kuriame vertinamas ABP 206 veiksmingumas, saugumas ir imunogeniškumas, palyginti su OPDIVO® (nivolumabu) gydymui nepasirengusiems asmenims, sergantiems neišplitusia ar metastazavusia melanoma. Protokolo Nr. 20210031 |
| Fazė | III |
| Indikacija | I eilė, kai nerezektabili III / IV st |
| Intervencija | Nivolumabas vs biosimiliarus Nivolumabas |
| Komanda | PI-V. Urbonas. Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 6 |
| Tyrimo pabaiga | 2025-01 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Krūties vėžys |
| Tyrimo pavadinimas, protokolo nr. | CHAIMELEON dirbtinio intelekto įrankių perkėlimo iš laboratorijos į rinką spartinimas vėžio valdymui. Protokolo Nr. CHAIMELEON |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Krūties Ca |
| Intervencija | Radiologinių vaizdų ir klinik. duomenų surinkimas |
| Komanda | PI-J. Ušinskienė; Koordinatorius - I.R.Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 995 |
| Tyrimo pabaiga | 2025 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Krūties vėžys |
| Tyrimo pavadinimas, protokolo nr. | Atsitiktinių imčių III fazės tyrimas, pažasties operacija su pažasties limfmazgių, TAXIS |
| Fazė | III |
| Indikacija | Krūties Ca su kliniškai pakenktais lm |
| Intervencija | Operacija su pažasties lm disekcija arba be jos, po kurios taikoma spindulinė terapija |
| Komanda | PI- V. Ostapenko; Koordinatorius A. Šukštienė |
| Tyrimo būsena / Liko vietų | 44 |
| Tyrimo pabaiga | 2024-12 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Krūties vėžys |
| Tyrimo pavadinimas, protokolo nr. | Pažasties limfmazgių disekcijos sąsaja su onkologiniu saugumu pacientams. Protokolo Nr. OPBC-07/microNAC |
| Fazė | III |
| Indikacija | Krūties Ca, kai nustatoma likusių mikrometastazių po neoadjuvantinės chemoterapijos, kai taikyta pažasties disekacija arba be jos. |
| Intervencija | Duomenų rinkimas |
| Komanda | PI- V. Ostapenko; Koordinatorius I. R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 24 |
| Tyrimo pabaiga | 2024-12 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Skrandžio vėžys |
| Tyrimo pavadinimas, protokolo nr. | PIPAC |
| Fazė | Pilotinis |
| Indikacija | I eilė, HER2(-), metastazes tik pilvaplėvėje |
| Intervencija | PIPAC + FOLFOX |
| Komanda | PI – A. Baušys, Koordinatorius A. Šukštienė |
| Tyrimo būsena / Liko vietų | 15 |
| Tyrimo pabaiga | 2024 m. |
| Įtraukimą Vykdantis | Taip |
| Grupė | Skrandžio vėžys |
| Tyrimo pavadinimas, protokolo nr. | Epigenetiniai kraujyje laisvai cirkuliuojančios DNR žymenys ankstyvajai vėžio atkryčio diagnostikai. Protokolo Nr. EpiCancer2023 |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Planuojama perioperacinė chemoterapija |
| Intervencija | Kraujo ėminiai cfDNR nustatyti |
| Komanda | PI- A. Dulskas. Koordinatorius N. Kravčenko |
| Tyrimo būsena / Liko vietų | 20 |
| Tyrimo pabaiga | 2028 m. |
| Įtraukimą Vykdantis | Taip |
| Grupė | Storosios žarnos ir plonosios žarnos vėžys |
| Tyrimo pavadinimas, protokolo nr. | Epigenetiniai kraujyje laisvai cirkuliuojančios DNR žymenys ankstyvajai vėžio atkryčio diagnostikai. Protokolo Nr. EpiCancer2023. |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Planuojama neoadjuvantinė chemoterapija |
| Intervencija | Kraujo ėminiai cfDNR nustatyti |
| Komanda | PI - A. Dulskas. Koordinatorius N. Kravčenko |
| Tyrimo būsena / Liko vietų | 20 |
| Tyrimo pabaiga | 2028 m. |
| Įtraukimą Vykdantis | Taip |
| Grupė | Storosios žarnos ir plonosios žarnos vėžys |
| Tyrimo pavadinimas, protokolo nr. | CHAIMELEON dirbtinio intelekto įrankių perkėlimo iš laboratorijos į rinką spartinimas vėžio valdymui. Protokolo Nr. CHAIMELEON |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Storosios žarnos ir plonosios žarnos vėžio Ca |
| Intervencija | Radiologinių vaizdų ir klinik. duomenų surinkimas |
| Komanda | PI-J. Ušinskienė. Koordinatorius - I.R.Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 995 |
| Tyrimo pabaiga | 2025 m. |
| Įtraukimą Vykdantis | Taip |
| Grupė | Galvos kaklo vėžys |
| Tyrimo pavadinimas, protokolo nr. | Atviras I fazės daugiacentris, randomizuotas, dvigubai aklas tyrimas, kuriame vertinamas ABP 206 farmakokinetinis panašumas, palyginti su OPDIVO® (Nivolumabu), skirto III ar IV stadijos melanomai, sergantiems rezekuotomis melanomomis adjuvantinėje aplinkoje. Protokolo Nr. NECVAX-NEO1-LT |
| Fazė | I |
| Indikacija | Bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST |
| Intervencija | Papildoma geriamoji vakcina |
| Komanda | PI-V. Urbonas; Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 6 |
| Tyrimo pabaiga | 2026-11 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Prostatos vėžys |
| Tyrimo pavadinimas, protokolo nr. | CHAIMELEON dirbtinio intelekto įrankių perkėlimo iš laboratorijos į rinką spartinimas vėžio valdymui. Protokolo Nr. CHAIMELEON |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Prostatos Ca |
| Intervencija | Radiologinių vaizdų ir klinik. duomenų surinkimas |
| Komanda | PI-J. Ušinskienė. Koordinatorius - I.R.Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 995 |
| Tyrimo pabaiga | 2025 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Prostatos vėžys |
| Tyrimo pavadinimas, protokolo nr. | 3 fazės, atsitiktinių imčių, atviras MK-5684 ir alternatyvaus preparato abiraterono acetato arba enzalutamido tyrimas, skirtas tiriamiesiems, sergantiems metastazavusiu, kastracijai atspariu prostatos vėžiu (mKAPV), progresavusiu po ankstesnio gydymo vienu naujos kartos hormoniniu preparatu (NKHP) Protokolo Nr. MK5684-004 |
| Fazė | III |
| Indikacija | Kastracijai atsparus prostatos vėžys (mKAPV), progresavęs po ankstesnio gydymo vienu naujos kartos hormoniniu preparatu (NKHP) |
| Intervencija | MK-5684, abiraterono acetatas arba enzalutamidas |
| Komanda | PI - A. Ulys. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | 9 |
| Tyrimo pabaiga | 2026 m. |
| Įtraukimą Vykdantis | Taip |
| Grupė | Inkstų vėžys |
| Tyrimo pavadinimas, protokolo nr. | Atviras I fazės daugiacentris, randomizuotas, dvigubai aklas tyrimas, kuriame vertinamas ABP 206 farmakokinetinis panašumas, palyginti su OPDIVO® (Nivolumabu), skirto III ar IV stadijos melanomai, sergantiems rezekuotomis melanomomis adjuvantinėje aplinkoje. Protokolo Nr. NECVAX-NEO1-LT |
| Fazė | I |
| Indikacija | Bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST |
| Intervencija | Papildoma geriamoji vakcina |
| Komanda | PI-V. Urbonas; Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 6 |
| Tyrimo pabaiga | 2026-11 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Plaučių vėžys |
| Tyrimo pavadinimas, protokolo nr. | 3 fazės, atsitiktinių imčių, dvigubai koduotas, placebu ir aktyviuoju palyginamuoju preparatu kontroliuojamas klinikinis tyrimas, skirtas palyginti adjuvanto V940 (mRNR-4157) skyrimą kartu su pembrolizumabu ir adjuvanto placebo skyrimą kartu su pembrolizumabu dalyviams, sergantiems rezekuotu II, IIIA, IIIB (N2) stadijos nesmulkiųjų ląstelių plaučių vėžiu. Protokolo Nr. V940-002 |
| Fazė | III |
| Indikacija | NSLPV, išoperuotas (R0) II, IIIA, IIIB st, N2, I eilė |
| Intervencija | V940 + Pembro |
| Komanda | PI- V. Gedvilaitė. Koordinatorius - A. Šukštienė |
| Tyrimo būsena / Liko vietų | 4 |
| Tyrimo pabaiga | 2025 m. |
| Įtraukimą Vykdantis | Taip |
| Grupė | Plaučių vėžys |
| Tyrimo pavadinimas, protokolo nr. | Atviras I fazės daugiacentris, randomizuotas, dvigubai aklas tyrimas, kuriame vertinamas ABP 206 farmakokinetinis panašumas, palyginti su OPDIVO® (Nivolumabu), skirto III ar IV stadijos melanomai, sergantiems rezekuotomis melanomomis adjuvantinėje aplinkoje. Protokolo Nr. NECVAX-NEO1-LT Protokolo Nr. NECVAX-NEO1-LT |
| Fazė | I |
| Indikacija | NSCLC bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST |
| Intervencija | Papildoma geriamoji vakcina |
| Komanda | PI-V. Urbonas; Sub-I - E. Baltruškevičienė, L. Gatijatullin; Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 6 |
| Tyrimo pabaiga | 2026-11 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Plaučių vėžys |
| Tyrimo pavadinimas, protokolo nr. | CHAIMELEON dirbtinio intelekto įrankių perkėlimo iš laboratorijos į rinką spartinimas vėžio valdymui. Protokolo Nr. CHAIMELEON |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Plaučių Ca |
| Intervencija | Radiologinių vaizdų ir klinik. duomenų surinkimas |
| Komanda | PI-J. Ušinskienė. Koordinatorius - I. R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 995 |
| Tyrimo pabaiga | 2025 m. |
| Įtraukimą Vykdantis | Taip |
| Grupė | Plaučių vėžys |
| Tyrimo pavadinimas, protokolo nr. | Atviras, daugiacentris, 3 fazės atsitiktinių imčių, aktyviais lyginamaisiais metodais kontroliuojamas klinikinis tyrimas Pembrolizumabo (MK-3475) derinyje su Sacituzumab Govitecan, palyginti su MK-3475 monoterapija, kaip pirmos eilės gydymu sergant PD L1 TPS didesnis arba lygus 50 % metastazavusiu nesmulkialąsteliniu plaučių vėžiu (KEYNOTE D46/EVOKE-03). Protokolo Nr. MK-3475-D46 |
| Fazė | III |
| Indikacija | NSLPV, IV st, PD-L1>50%, I eilė |
| Intervencija | Pembro+sacituzumab govitekan |
| Komanda | PI – S. Cicėnas. Koordinatoriai - A. Šukštienė, I. R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 5 |
| Tyrimo pabaiga | 2025-03 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Kiti solidiniai navikai |
| Tyrimo pavadinimas, protokolo nr. | Atvirasis, I fazės daugiacentris, klinikinis tyrimas siekiant įvertinti NECVAX-NEO1, Protokolo Nr. NECVAX-NEO1-LT |
| Fazė | I |
| Indikacija | Bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST |
| Intervencija | Papildoma geriamoji vakcina |
| Komanda | PI-V. Urbonas; Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 6 |
| Tyrimo pabaiga | 2026-11 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Kiti solidiniai navikai |
| Tyrimo pavadinimas, protokolo nr. | Europos onkologinio gyvenimo kokybės priemonių rinkinio patvirtinimas. Europos pilotinė apklausa. Protokolo Nr. EUonQoL |
| Fazė | Biomedicininis tyrimas |
| Indikacija | Kiti solidiniai navikai - aktyvus gydymas, stebėsena arba paliatyvus gydymas |
| Intervencija | Neintervencinis, stebimasis |
| Komanda | PI- A. Dulskas; Koordinatoriai N. Kravčenko, I. R. Kasiliauskaitė |
| Tyrimo būsena / Liko vietų | 79 |
| Tyrimo pabaiga | 2024-11 |
| Įtraukimą Vykdantis | Taip |
| Grupė | Tyrimo pavadinimas, protokolo nr. | Fazė | Indikacija | Intervencija | Komanda | Tyrimo būsena / Liko vietų | Tyrimo pabaiga | Įtraukimą Vykdantis | |
| Melanoma | Atsitiktinių imčių, lygiagrečių grupių tyrimas, skirtas palyginti GME75. Protokolo Nr. CGME751A12101 | I | IIB, IIC, III st. melanoma, 2-13 sav. po rezekcijos | GME751/Pembrolizumab | PI-V. Urbonas. Koordinatoriai- A. Šukštienė, I.R. Kasiliauskaitė | 8 | 2025-06 | Taip | |
| Melanoma | Atviras I fazės daugiacentris, randomizuotas, dvigubai aklas tyrimas, kuriame vertinamas ABP 206 farmakokinetinis panašumas, palyginti su OPDIVO® (Nivolumabu), skirto III ar IV stadijos melanomai, sergantiems rezekuotomis melanomomis adjuvantinėje aplinkoje. Protokolo Nr. NECVAX-NEO1-LT |
I | Bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST | Papildoma geriamoji vakcina | PI-V. Urbonas. Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė | 6 | 2026-11 | Taip | |
| Melanoma | Epigenetiniai kraujyje laisvai cirkuliuojančios DNR žymenys ankstyvajai vėžio atkryčio diagnostikai. Protokolo Nr. EpiCancer2023 | Biomedicininis tyrimas | Planuojama perioperacinė chemoterapija | Kraujo ėminiai cfDNR nustatyti | PI - A. Dulskas, Koordinatorius - N. Kravčenko | 20 | 2028 m. | Taip | |
| Kiaušidžių vėžys | Atsitiktinių imčių klinikinis tyrimas palaikomajai terapijai olaparibu, durvalumabu, NSGO-CTU-DOVACC. Protokolo Nr. NSGO-CTU-DOVACC | III | Platinai jautrus, I arba II atkrytis, BRCA (-) | Palaikomasis gydymas olaparibu+/-durvaliumabu+/-UV1 | PI- B. Brasiūnienė; Koordinatorius A. Šukštienė | 3 | 2026-12 | Taip | |
| Melanoma | Atsitiktinių imčių dvigubai aklas tyrimas, kuriame vertinamas ABP 206 veiksmingumas, saugumas ir imunogeniškumas, palyginti su OPDIVO® (nivolumabu) gydymui nepasirengusiems asmenims, sergantiems neišplitusia ar metastazavusia melanoma. Protokolo Nr. 20210031 | III | I eilė, kai nerezektabili III / IV st | Nivolumabas vs biosimiliarus Nivolumabas | PI-V. Urbonas. Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė | 6 | 2025-01 | Taip | |
| Krūties vėžys | CHAIMELEON dirbtinio intelekto įrankių perkėlimo iš laboratorijos į rinką spartinimas vėžio valdymui. Protokolo Nr. CHAIMELEON | Biomedicininis tyrimas | Krūties Ca | Radiologinių vaizdų ir klinik. duomenų surinkimas | PI-J. Ušinskienė; Koordinatorius - I.R.Kasiliauskaitė | 995 | 2025 | Taip | |
| Krūties vėžys | Atsitiktinių imčių III fazės tyrimas, pažasties operacija su pažasties limfmazgių, TAXIS | III | Krūties Ca su kliniškai pakenktais lm | Operacija su pažasties lm disekcija arba be jos, po kurios taikoma spindulinė terapija | PI- V. Ostapenko; Koordinatorius A. Šukštienė | 44 | 2024-12 | Taip | |
| Krūties vėžys | Pažasties limfmazgių disekcijos sąsaja su onkologiniu saugumu pacientams. Protokolo Nr. OPBC-07/microNAC | III | Krūties Ca, kai nustatoma likusių mikrometastazių po neoadjuvantinės chemoterapijos, kai taikyta pažasties disekacija arba be jos. | Duomenų rinkimas | PI- V. Ostapenko; Koordinatorius I. R. Kasiliauskaitė | 24 | 2024-12 | Taip | |
| Skrandžio vėžys | PIPAC | Pilotinis | I eilė, HER2(-), metastazes tik pilvaplėvėje | PIPAC + FOLFOX | PI – A. Baušys, Koordinatorius A. Šukštienė | 15 | 2024 m. | Taip | |
| Skrandžio vėžys | Epigenetiniai kraujyje laisvai cirkuliuojančios DNR žymenys ankstyvajai vėžio atkryčio diagnostikai. Protokolo Nr. EpiCancer2023 | Biomedicininis tyrimas | Planuojama perioperacinė chemoterapija | Kraujo ėminiai cfDNR nustatyti | PI- A. Dulskas. Koordinatorius N. Kravčenko | 20 | 2028 m. | Taip | |
| Storosios žarnos ir plonosios žarnos vėžys | Epigenetiniai kraujyje laisvai cirkuliuojančios DNR žymenys ankstyvajai vėžio atkryčio diagnostikai. Protokolo Nr. EpiCancer2023. | Biomedicininis tyrimas | Planuojama neoadjuvantinė chemoterapija | Kraujo ėminiai cfDNR nustatyti | PI - A. Dulskas. Koordinatorius N. Kravčenko | 20 | 2028 m. | Taip | |
| Storosios žarnos ir plonosios žarnos vėžys | CHAIMELEON dirbtinio intelekto įrankių perkėlimo iš laboratorijos į rinką spartinimas vėžio valdymui. Protokolo Nr. CHAIMELEON | Biomedicininis tyrimas | Storosios žarnos ir plonosios žarnos vėžio Ca | Radiologinių vaizdų ir klinik. duomenų surinkimas | PI-J. Ušinskienė. Koordinatorius - I.R.Kasiliauskaitė | 995 | 2025 m. | Taip | |
| Galvos kaklo vėžys | Atviras I fazės daugiacentris, randomizuotas, dvigubai aklas tyrimas, kuriame vertinamas ABP 206 farmakokinetinis panašumas, palyginti su OPDIVO® (Nivolumabu), skirto III ar IV stadijos melanomai, sergantiems rezekuotomis melanomomis adjuvantinėje aplinkoje. Protokolo Nr. NECVAX-NEO1-LT |
I | Bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST | Papildoma geriamoji vakcina | PI-V. Urbonas; Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė | 6 | 2026-11 | Taip | |
| Prostatos vėžys | CHAIMELEON dirbtinio intelekto įrankių perkėlimo iš laboratorijos į rinką spartinimas vėžio valdymui. Protokolo Nr. CHAIMELEON | Biomedicininis tyrimas | Prostatos Ca | Radiologinių vaizdų ir klinik. duomenų surinkimas | PI-J. Ušinskienė. Koordinatorius - I.R.Kasiliauskaitė | 995 | 2025 | Taip | |
| Prostatos vėžys | 3 fazės, atsitiktinių imčių, atviras MK-5684 ir alternatyvaus preparato abiraterono acetato arba enzalutamido tyrimas, skirtas tiriamiesiems, sergantiems metastazavusiu, kastracijai atspariu prostatos vėžiu (mKAPV), progresavusiu po ankstesnio gydymo vienu naujos kartos hormoniniu preparatu (NKHP) Protokolo Nr. MK5684-004 | III | Kastracijai atsparus prostatos vėžys (mKAPV), progresavęs po ankstesnio gydymo vienu naujos kartos hormoniniu preparatu (NKHP) | MK-5684, abiraterono acetatas arba enzalutamidas | PI - A. Ulys. Koordinatorius - A. Šukštienė | 9 | 2026 m. | Taip | |
| Inkstų vėžys | Atviras I fazės daugiacentris, randomizuotas, dvigubai aklas tyrimas, kuriame vertinamas ABP 206 farmakokinetinis panašumas, palyginti su OPDIVO® (Nivolumabu), skirto III ar IV stadijos melanomai, sergantiems rezekuotomis melanomomis adjuvantinėje aplinkoje. Protokolo Nr. NECVAX-NEO1-LT |
I | Bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST | Papildoma geriamoji vakcina | PI-V. Urbonas; Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė | 6 | 2026-11 | Taip | |
| Plaučių vėžys | 3 fazės, atsitiktinių imčių, dvigubai koduotas, placebu ir aktyviuoju palyginamuoju preparatu kontroliuojamas klinikinis tyrimas, skirtas palyginti adjuvanto V940 (mRNR-4157) skyrimą kartu su pembrolizumabu ir adjuvanto placebo skyrimą kartu su pembrolizumabu dalyviams, sergantiems rezekuotu II, IIIA, IIIB (N2) stadijos nesmulkiųjų ląstelių plaučių vėžiu. Protokolo Nr. V940-002 | III | NSLPV, išoperuotas (R0) II, IIIA, IIIB st, N2, I eilė | V940 + Pembro | PI- V. Gedvilaitė. Koordinatorius - A. Šukštienė | 4 | 2025 m. | Taip | |
| Plaučių vėžys | Atviras I fazės daugiacentris, randomizuotas, dvigubai aklas tyrimas, kuriame vertinamas ABP 206 farmakokinetinis panašumas, palyginti su OPDIVO® (Nivolumabu), skirto III ar IV stadijos melanomai, sergantiems rezekuotomis melanomomis adjuvantinėje aplinkoje. Protokolo Nr. NECVAX-NEO1-LT Protokolo Nr. NECVAX-NEO1-LT |
I | NSCLC bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST | Papildoma geriamoji vakcina | PI-V. Urbonas; Sub-I - E. Baltruškevičienė, L. Gatijatullin; Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė | 6 | 2026-11 | Taip | |
| Plaučių vėžys | CHAIMELEON dirbtinio intelekto įrankių perkėlimo iš laboratorijos į rinką spartinimas vėžio valdymui. Protokolo Nr. CHAIMELEON | Biomedicininis tyrimas | Plaučių Ca | Radiologinių vaizdų ir klinik. duomenų surinkimas | PI-J. Ušinskienė. Koordinatorius - I. R. Kasiliauskaitė | 995 | 2025 m. | Taip | |
| Plaučių vėžys | Atviras, daugiacentris, 3 fazės atsitiktinių imčių, aktyviais lyginamaisiais metodais kontroliuojamas klinikinis tyrimas Pembrolizumabo (MK-3475) derinyje su Sacituzumab Govitecan, palyginti su MK-3475 monoterapija, kaip pirmos eilės gydymu sergant PD L1 TPS didesnis arba lygus 50 % metastazavusiu nesmulkialąsteliniu plaučių vėžiu (KEYNOTE D46/EVOKE-03). Protokolo Nr. MK-3475-D46 |
III | NSLPV, IV st, PD-L1>50%, I eilė | Pembro+sacituzumab govitekan | PI – S. Cicėnas. Koordinatoriai - A. Šukštienė, I. R. Kasiliauskaitė | 5 | 2025-03 | Taip | |
| Kiti solidiniai navikai | Atvirasis, I fazės daugiacentris, klinikinis tyrimas siekiant įvertinti NECVAX-NEO1, Protokolo Nr. NECVAX-NEO1-LT | I | Bent 3 mėn. taikoma imunoterapija ir gauta stabili liga/ dalinis atsakas; matuojama liga pagal RECIST | Papildoma geriamoji vakcina | PI-V. Urbonas; Koordinatoriai - A. Šukštienė, I.R. Kasiliauskaitė | 6 | 2026-11 | Taip | |
| Kiti solidiniai navikai | Europos onkologinio gyvenimo kokybės priemonių rinkinio patvirtinimas. Europos pilotinė apklausa. Protokolo Nr. EUonQoL | Biomedicininis tyrimas | Kiti solidiniai navikai - aktyvus gydymas, stebėsena arba paliatyvus gydymas | Neintervencinis, stebimasis | PI- A. Dulskas; Koordinatoriai N. Kravčenko, I. R. Kasiliauskaitė | 79 | 2024-11 | Taip |
__________________________


Informuotumo apie prostatos vėžį didinimas ir atrankinės patikros iniciatyva (PRAISE-U) yra konsorciumas, vadovaujamas Europos urologų asociacijos (angl. European Associacion of Urology, EAU), skirtas sumažinti sergamumą prostatos vėžiu ir mirtingumą nuo jo Europos Sąjungoje. Šis konsorciumas ir projektas siekia suteikti tvirtus įrodymus dėl individualia rizika paremtos strategijos taikymo ankstyvoje prostatos vėžio diagnostikoje. VšĮ Nacionalinio vėžio instituto gydytojai, mokslininkai ir kiti specialistai yra šio biomedicininio tyrimo tyrėjai.
Biomediciniam tyrimui Vilniaus regioninis biomedicininių tyrimų etikos komitetas yra išdavęs leidimą.
Biomedicininio tyrimo tikslai:
- sumažinti sergamumą ir mirtingumą nuo prostatos vėžio ES valstybėse narėse, pasitelkiant išmanią ankstyvą diagnostiką;
- skatinti ankstyvą prostatos vėžio nustatymą ir diagnozavimą, taikant rizika pagrįstas patikros programas;
- suderinti protokolus ir gaires visose ES valstybėse narėse ir sudaryti sąlygas rinkti bei platinti atitinkamus duomenis, siekiant sumažinti sergamumą ir mirtingumą nuo prostatos vėžio Europoje.
Projektas susideda iš šešių darbinių paketų, vienas iš jų – pilotinių tyrimų vykdymas projekto centruose. Pilotinio tyrimo centruose pacientai bus kviečiami sudalyvauti organizuotoje profilaktinėje patikroje dėl prostatos vėžio (Lietuvoje tai standartinė klinikinė praktika nuo 2006 m.). Pacientams bus atliekamas vertinimas pagal riziką, prostatos magnetinio rezonanso tomografijos tyrimą ir biopsiją profilaktinės patikros programos rėmuose.
Biomedicininio tyrimo uždaviniai:
- įgyvendinti, įvertinti Europos urologų asociacijos ir PRAISE-U konsorciumo rekomenduojamą individualizuota rizika paremtos profilaktinės patikros dėl prostatos vėžio modelį Lietuvoje, vykdomo procesą ir rezultatų rodiklius;
- gauti suinteresuotųjų šalių įžvalgas apie Europos urologų asociacijos ir PRAISE-U konsorciumo rekomenduojamos individualizuota rizika paremtos profilaktinės patikros dėl prostatos vėžio modelį, siekiant padidinti profilaktinės patikros svarbą, padidinti dalyvavimą patikroje, sumažinti patikros vykdymo rizikas ir remti nuolatinį patikros tobulinimą;
- ištirti suinteresuotųjų šalių (sveikatos priežiūros paslaugų teikėjų) požiūrį į Europos urologų asociacijos ir PRAISE-U konsorciumo rekomenduojamos individualizuota rizika paremtos profilaktinės patikros dėl prostatos vėžio modelį, prieš šį tyrimą ir po šio tyrimo (naudojant kiekybinius klausimynus ir tikslinių grupių interviu);
- ištirti psichosocialinį profilaktinės patikros poveikį populiaciniu pagrindu individualizuota rizika paremtos profilaktinės patikros dėl prostatos vėžio rizikos grupėms;
- įvertinti Europos urologų asociacijos ir PRAISE-U konsorciumo rekomenduojamos individualizuota rizika paremtos profilaktinės patikros dėl prostatos vėžio modelio įgyvendinimo sąnaudas ir poveikį, palyginti su dabartine standartine praktika.
Norėdami dalyvauti šiame biomedicininiame tyrime Jūs turite būti:
- 50–69 m. amžiaus vyras, kuriam pirminės sveikatos priežiūros paslaugos teikiamos Vilniaus universiteto ligoninės Santaros klinikų poliklinikoje ar Šeškinės poliklinikoje;
- asmuo, kuriam anksčiau nebuvo nustatytas prostatos vėžys;
- iki dalyvavimo tyrime pradžios pusę metų Jums nebuvo atliktas prostatos magnetinio rezonanso tomografijos tyrimas,
- pasiruošęs pasirašyti informuoto asmens sutikimo formą bei leisti tyrėjams naudoti Jūsų sveikatos duomenis;
- pasiruošę negauti tiesioginės naudos dalyvaudami tyrime, suprasti, jog Jūsų dalyvavimas padės pagerinti ir nustatyti aiškias profilaktinės patikros dėl prostatos vėžio vykdymo rekomendacijas Europos Sąjungoje;
- pasiruošęs dalyvaudamas šiame tyrime patirti nepatogumų, tokių kaip veninio kraujo paėmimas ištyrimui, sugaištas laikas pildant psichosocialinius klausimynus konsultacijos metu.
Visa kita praktika atliekama tyrimo metu yra standartinė ir reglamentuota pagal LR įstatymus, poįstatyminius teisės aktus ir LR SAM ministro įsakymus. Dalyvavimas biomedicininiame tyrime nekelia jokios papildomos rizikos tiriamiesiems. Dalyvavimas tyrime nedarys jokios įtakos tiriamųjų gydymo planui, biomedicininio tyrimo tikslais nebus atliekamos jokios papildomos procedūros ir jokios žalos tiriamiesiems negali būti.
Jei Jums bus nustatyta didesnė nei 3 ng/ml prostatos specifinio antigeno koncentracija, būsite nukreiptas į VšĮ Nacionalinį vėžio institutą, kur Jums bus išmatuotas prostatos tūris ir įvertinta rizika diagnozuoti prostatos vėžį. Esant vidutinei ar aukštai rizikai, Jums bus atliekamas prostatos magnetinis rezonansas. Nepriklausomai nuo to, ar Jums bus padidinta prostatos specifinio antigeno koncentracija kraujyje, visiems tiriamiesiems bus taikoma įprastinė sveikatos priežiūra.
Jei turite klausimų susijusių su PRAISE-U tyrimu, prašome kreiptis į:
Pagrindinį tyrėją Doc. Dr. Aušvydą Patašių, el. paštu ausvydas.patasius![]() nvi.lt
nvi.lt
Tyrėją gyd. Ugnę Mickevičiūtę, el. paštu ugne.mickeviciute![]() nvi.lt
nvi.lt
PRAISE-U algoritmas
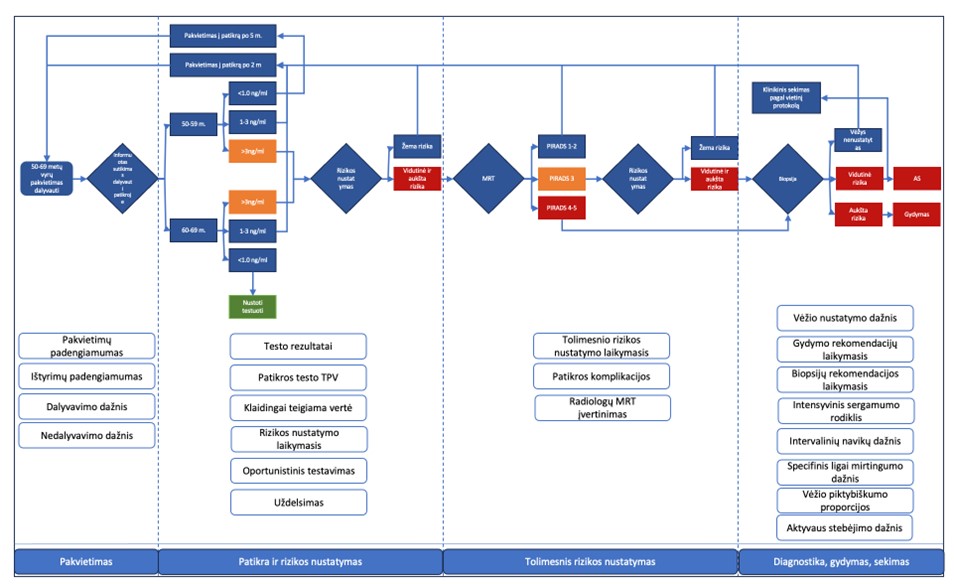
Atnaujinta 2025-01-10 10:06
Svarbu žinoti:



